Đáp án đề thi thử THPT Quốc gia môn Hóa lần 2 năm 2016 – THPT Yên Lạc, tỉnh Vĩnh Phúc, các em theo dõi dưới đây:
Xem thêm: Đề thi thử THPT Quốc gia môn Hóa
|
SỞ GD & ĐT VĨNH PHÚC TRƯỜNG THPT YÊN LẠC (Đề thi có 04 trang) |
ĐỀ THI KHẢO SÁT CHẤT LƯỢNG LẦN 2 – LỚP 12 NĂM HỌC: 2015 – 2016 ĐỀ THI MÔN: HÓA HỌC Thời gian làm bài: 90 phút; (50 câu trắc nghiệm) |
Cho: H = 1; C = 12; N = 14; O = 16; Na = 23; Mg = 24; Al = 27; S = 32; P = 31; Cl = 35,5; K = 39; Be = 9; Li = 7; Ca = 40; Ba = 137; Cr = 52; F = 19; Mn = 55; Ni =59; Fe = 56; Cu = 64; Zn = 65; Br = 80; Ag = 108; Ba = 137; I = 127; Si = 28; Rb = 85.
Câu 1: Trong dãy các chất sau: (1): CH
NH
, (2): CH
-NH-CH
, (3): NH
, (4): C
H
NH
, (5): KOH. Dãy sắp xếp các chất theo chiều tăng dần tính bazơ là
A. (5) < (4) < (3) < (1) < (2). B. (5) < (4) < (3) < (2) < (1).
C. (4) < (3) < (1) < (2) < (5). D. (4) < (3) < (2) < (1) < (5).
Câu 2: Kim cương có cấu tạo kiểu mạng tinh thể
A. nguyên tử. B. kim loại. C. phân tử. D. ion.
Câu 3: Cho 18,4 gam hỗn hợp X gồm Cu
S, CuS, FeS
và FeS tác dụng hết với HNO
(đặc nóng, dư) thu được V lít khí chỉ có NO
(ở đktc, sản phẩm khử duy nhất ) và dung dịch Y. Cho toàn bộ Y vào một lượng dư dung dịch BaCl
, thu được 46,6 gam kết tủa; còn khi cho toàn bộ Y tác dụng với dung dịch NH
dư thu được 10,7 gam kết tủa. Giá trị của V là
A. 24,64. B. 11,2. C. 16,8. D. 38,08.
Câu 4: Cho sơ đồ phản ứng sau:
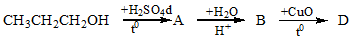
(A, B, D là những sản phẩm chính). Xác định công thức cấu tạo của D?
A. CH
COOH. B. CH
CH
CHO. C. CH
CH
COOH. D. CH
COCH
.
Câu 5: Phân tử tinh bột được cấu tạo từ
A. các gốc fructozơ. B. các gốc glucozơ. C. các gốc glucozơ. D. các gốc fructozơ.
Câu 6: Cho các chất sau: Al(OH)
(1), H
O (2), NaHCO
(3), CuO (4), Na
CO
(5). Theo thuyết Bronsted, trong dãy các chất sau đây, dãy chất nào mà tất cả các chất đều là lưỡng tính ?
A. (1), (3). B. (1), (2), (3), (4) C. (1), (2), (3), (4), (5). D. (1), (2), (3).
Câu 7: Để nhận biết ba dung dịch H
NCH
COOH, CH
CH
COOH và CH
NH
người ta dùng một hoá chất duy nhất nào sau đây?
A. Quỳ tím. B. Dung dịch HCl. C. Dung dịch H
SO
. D. Dung dịch NaOH.
Câu 8: Một loại phân kali có thành phần chính là KCl (còn lại là tạp chất không chứa kali) được sản xuất từ quặng xinvinit có độ dinh dưỡng 55 %. Phần trăm khối lượng của KCl trong loại phân kali đó là
A. 88,52 %. B. 87,18 %. C. 65,75 %. D. 95,51 %.
Câu 9: Cho 5,9 gam amin đơn chất X tác dụng vừa đủ với dung dịch HCl, sau phản ứng xảy ra hoàn toàn thu được dung dịch Y. Làm bay hơi dung dịch Y được 9,55 gam muối khan. Số công thức cấu tạo ứng với công thức phân tử của X là
A. 4. B. 3. C. 5. D. 2.
Câu 10: Cho các dung dịch sau: KCl, AlCl
, Na
CO
, NH
NO
, Na
S, Fe
(SO
)
, BaCl
, KHSO
. Nhận xét đúng là
A. Có 4 dung dịch không làm đổi màu quỳ tím. B. Có 3 dung dịch có pH = 7.
C. Có 5 dung dịch có pH < 7. D. Có 2 dung dịch làm quỳ tím hóa xanh.
Câu 11: Cho 18,5 gam hỗn hợp gồm Fe và Fe
O
tác dụng với 200 ml dung dịch HNO
loãng, nóng, khuấy đều đến phản ứng hoàn toàn thu được 2,24 lít khí NO duy nhất (ở đktc), dung dịch X và 1,46 gam kim loại dư. Tính nồng độ mol của dung dịch HNO
?
A. 3,2 M. B. 3,35 M. C. 3,3 M. D. 3,4 M.
Câu 12: Axit fomic phản ứng được với tất cả các chất trong nhóm chất nào sau đây?
A. Na, Cu(OH)
, AgNO
/NH
. B. Ag, AgNO
/NH
, Cu(OH)
.
C. Zn, H
SO
, AgNO
/NH
. D. Cu, NaOH, Cu(OH)
.
Câu 13: Cho 26,4 gam hỗn hợp hai chất hữu cơ có cùng công thức phân tử C
H
O
tác dụng với dung dịch NaOH vừa đủ, thu được dung dịch X chứa 28,8 gam hỗn hợp muối và m gam ancol Y. Đun Y với dung dịch H
SO
đặc ở nhiệt độ thích hợp, thu được chất hữu cơ Z có tỉ khối hơi so với Y bằng 0,7. Biết các phản ứng xảy ra hoàn toàn. Giá trị của m là
A. 6,0. B. 6,4. C. 9,6. D. 4,6.
Câu 14: Có các nhận định sau:
(1) Lipit là một loại chất béo.
(2) Lipit gồm chất béo, sáp, sterit, photpholipit,….
(3) Chất béo là các chất lỏng.
(4) Chất béo chứa các gốc axit không no thường là chất lỏng ở nhiệt độ thường.
(5) Phản ứng thủy phân chất béo trong môi trường kiềm là phản ứng thuận nghịch.
(6) Chất béo là thành phần chính của dầu mỡ động,thực vật.
Các nhận định đúng là
A. 3, 4, 5. B. 2, 4, 6. C. 1, 2, 4, 5. D. 1, 2, 4, 6.
Câu 15: Đốt cháy hoàn toàn 3 lít hỗn hợp X gồm 2 anken kế tiếp nhau trong dãy đồng đẳng cần vừa đủ 10,5 lít O
(các thể tích khí đo trong cùng điều kiện nhiệt độ, áp suất). Hiđrat hóa hoàn toàn X trong điều kiện thích hợp thu được hỗn hợp ancol Y, trong đó khối lượng ancol bậc hai bằng 6/13 lần tổng khối lượng các ancol bậc một. Phần trăm khối lượng của ancol bậc một (có số nguyên tử cacbon lớn hơn) trong Y là
A. 7,89 %. B. 31,58 %. C. 10,88 %. D. 46,43 %.
Câu 16: Cho phản ứng : Br
+ HCOOH 2HBr + CO
. Nồng độ ban đầu của Br
là a mol/lít, sau 50 giây nồng độ Br
còn lại là 0,01 mol/lít. Tốc độ trung bình của phản ứng trên tính theo Br
là 4.10
mol/(l.s). Giá trị của a là
A. 0,018. B. 0,014. C. 0,016. D. 0,012.
Câu 17: Tơ nào sau đây là tơ bán tổng hợp?
A. Tơ nilon-6. B. Tơ nitron. C. Tơ visco. D. Tơ tằm.
Câu 18: Cho 200 ml dung dịch H
PO
1M vào 250 ml dung dịch hỗn hợp NaOH 0,5M và KOH 1,5. Sau khi phản ứng hoàn toàn thu được dung dịch X. Số gam muối có trong dung dịch X là
A. 38,4 gam. B. 32,6 gam. C. 36,6 gam. D. 40,2 gam.
Câu 19: Trong các nhóm chất sau, nhóm nào mà tất cả các chất đều phản ứng thế với clo khi có mặt của ánh sáng khuếch tán ?
A. Metan, etan, benzen. B. Metan, etan, etilen.
C. Metan, etan, stiren. D. Metan, toluen, etan.

Câu 23: Hòa tan hoàn toàn 20,88 gam một oxit sắt bằng dung dịch H
SO
đặc nóng thu được dung dịch X vầ 3,248 lít khí SO
(sản phẩm khử duy nhất, ở đktc). Cô cạn dung dịch X thu được m gam muối sunfat khan. Giá trị của m là
A. 52,2. B. 54,0. C. 48,4. D. 58,0.
Câu 24: Kim loại dẫn điện tốt nhất là
A. Ag. B. Cu. C. Al. D. Au.
Câu 25: Trong các thí nghiệp sau:
(1) Cho SiO
tác dụng với axit HF. (2) Cho khí SO
tác dụng với khí H
S.
(3) Cho khí NH
tác dụng với CuO đun nóng. (4) Cho CaOCl
tác dụng với HCl đặc.
(5) Cho Si đơn chất tác dụng với dung dịch NaOH. (6) Cho khí O
tác dụng với Ag.
(7) Cho dung dịch NH
Cl tác dụng với dung dịch NaNO
đun nóng.
Số thí nghiệm tạo ra đơn chất là
A. 4. B. 5. C. 7. D. 6.
Câu 26: Trong phòng thí nghiệm HX được điều chế từ phản ứng sau:
NaX
+ H
SO
NaHSO
(hoặc Na
SO
) + HX
Hãy cho biết phương pháp trên có thể dùng để điều chế được dãy HX nào sau đây ?
A. HF, HCl, HBr, HI. B. HF, HCl, HNO
. C. HCl, HBr, HI. D. HBr và HI.
Câu 27: Tripeptit mạch hở X và tetrapeptit mạch hở Y đều được cấu tạo từ một aminoaxit no, mạch hở có 1 nhóm -COOH và 1 nhóm -NH
. Đốt cháy hoàn toàn 0,1 mol X thu được sản phẩm gồm CO
, H
O, N
trong đó tổng khối lượng của CO
và H
O là 36,3 gam. Nếu đốt cháy hoàn toàn 0,2 mol Y cần số mol O
là
A. 1,875 B. 3,375 C. 2,8 D. 1,8
Câu 28: Điện phân 150ml dd AgNO
1M với điện cực trơ trong t giờ, cường độ dòng điện không đổi 1,34A (hiệu suất quá trình điện phân là 100%) thu được chất rắn X, dd Y và khí Z. Cho 13 gam Fe vào dd Y , sau khi các phản ứng kết thúc thu được 14,9 gam hỗn hợp kim loại và khí NO (sản phẩm khử duy nhất của N
). Giá trị của t là
A. 1,0. B. 1,5. C. 3,0. D. 2,0.
Câu 29: Cho dung dịch A chứa H
SO
0,1 M; HNO
0,2 M và HCl 0,3 M. Trộn 300 ml dung dịch A với V lít dung dịch B gồm NaOH 0,2 M và KOH 0,29 M thu được dung dịch C có pH = 2. Giá trị của V là
A. 0,441. B. 0,134. C. 0,424. D. 0,414.
Câu 30: Công thức của metyl fomat là
A. HCOOC
H
. B. CH
COOCH
. C. HCOOCH
. D. CH
COOH.
Câu 31: Hòa tan hoàn toàn 8,8 gam hợp kim Mg – Cu bằng axit HNO
, sau phản ứng thu được 4,48 lít hỗn hợp khí B gồm NO và NO
(ở đktc, ngoài ra không còn sản phẩm khử nào khác). Biết tỉ khối của B so với H
bằng 19. Thành phần của Mg trong hợp kim là
A. 27,27 %. B. 22,77 %. C. 72,72 %. D. 50,00 %.
Câu 32: Trong những đồng phân mạch hở của C
H
có bao nhiêu chất khi cộng Br
theo tỉ lệ mol 1 : 1 thì tạo thành cặp đồng phân cis – trans ?
A. 3 chất. B. 4 chất. C. 5 chất. D. 6 chất.
Câu 33: Trộn 0,05 mol HCHO với một anđehit D thu được hỗn hợp X. Cho hỗn hợp X tác dụng với dung dịch AgNO
/NH
dư thu được 25,92 gam Ag. Mặt khác khi đốt hoàn toàn X thu được 1,568 lít CO
(ở đktc). Xác định công thức cấu tạo của D ?
A. OHC-CH
-CHO. B. OHC-CHO. C. CH
-CH
-CHO. D. CH
CHO.
Câu 34: Khi thủy phân một phân tử peptit X thu được một phân tử glyxin, hai phân tử alanin và một phân tử valin. Số đồng phân vị trí của peptit X là
A. 10. B. 6. C. 12. D. 24.
Câu 35: Cho 8,8 gam anđehit axetic (CH
CHO) tham gia phản ứng tráng gương trong dung dịch AgNO
/NH
dư thì thu được m gam Ag. Giá trị của m là
A. 21,6. B. 4,32. C. 43,2. D. 10,8.
Câu 36: Đốt cháy m gam hỗn hợp X gồm hai ancol kế tiếp nhau trong dãy đồng đẳng, thu được 4,48 lít khí CO
(đktc) và 5,85 gam H
O. Mặt khác, nếu cho 2m gam X đi qua CuO ( dư ) nung nóng, rồi cho toàn bộ lượng anđehit sinh ra tác dụng với AgNO
/NH
thì thu được x gam Ag. Biết các phản ứng xảy ra hoàn toàn. Giá trị của x là
A. 75,6. B. 27,0. C. 54,0. D. 37,8.
Câu 37: Cho 3,24 gam Al
(SO
)
phản ứng với 25 ml dung dịch NaOH thu được 0,78 gam kết tủa trắng. Xác định nồng độ mol dung dịch NaOH đã dùng ?
A. 1,2M và 2,4M. B. 1,2M và 2,8M. C. 1,2M. D. 2,8M.
Câu 38: Cho hỗn hợp X gồm Al và Al
O
có tỷ lệ khối lượng tương ứng là 0,18 : 1,02. Cho X tan trong dung dịch NaOH vừa đủ thu được dung dịch Y và 0,672 lít khí H
(ở đktc). Cho Y tác dụng với 200 ml dung dịch HCl được kết tủa Z. Nung Z ở nhiệt độ cao đến khối lượng không đổi được 3,57 gam chất rắn. Nồng độ mol của dung dịch HCl là
A. 0,07 M hoặc 0,09 M. B. 0,35 M hoặc 0,45 M.
C. 0,07 M hoặc 0,11 M. D. 0,35 M hoặc 0,55 M.
Câu 39: Nhiệt phân hoàn toàn 18,8 gam Cu(NO
)
ta thu được sản phẩm khí, dẫn vào nước để được 200 ml dung dịch X. Tính nồng độ mol của dung dịch X?
A. 0,5 M. B. 2,0 M. C. 1,0 M. D. 1,5 M.
Câu 40: Cho dãy các chất sau: axit axetic, anđehit fomic, ancol benzylic, cumen, etylaxetat, glucozơ, etylamin. Số chất trong dãy có thể tác dụng với Cu(OH)
là
A. 4. B. 2. C. 3. D. 5.
Câu 41: Một dung dịch gồm: 0,03 mol, K
; 0,04 mol Ba
; 0,05 mol HCO
và a mol ion X (bỏ qua sự điện li của nước). Ion X và giá trị của a lần lượt là
A. Cl
và 0,03. B. NO
và 0,06. C. OH
và 0,06. D. SO
và 0,03.
Câu 42: Cho hình vẽ về cách thu khí dời nước như sau:
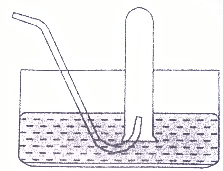
Hình vẽ bên có thể áp dụng để thu được những khí nào trong các khí sau đây ?
A. NH
, O
, N
, HCl, CO
. B. H
, N
, O
, CO
, HCl, H
S.
C. CO
, O
, N
, H
. D. NH
, HCl, CO
, SO
, Cl
.
Câu 43: Trong số các loại hợp chất sau, loại hợp chất nào được gọi là “mang hương sắc cho đời” ?
A. Hiđrocacbon thơm. B. Tecpen. C. Este. D. Lipit.
Câu 44: Hợp chất nào sau đây thuộc loại đipeptit ?
A. H
N-CH
-CO-NH-CH(CH
)-COOH. B. H
N-CH
-NH-CH
COOH.
C. H
N-CH
-CH
-CO-NH-CH
-CH
-COOH. D. H
N-CH
-CH
-CO-NH-CH
-COOH.
Câu 45: Một nguyên tử có tổng số e ở 2 lớp M và N là 9. Vị trí của nguyên tố đó trong bảng tuần hoàn là
A. Chu kì 3, nhóm IIA. B. Chu kì 4, nhóm IA. C. Chu kì 4, nhóm IIA. D. Chu kì 4, nhóm IA.
Câu 46: Cho phản ứng: Fe + X FeCl
+ …Chất X nào sau đây đã chọn không đúng?
A. HCl. B. CuCl
. C. Cl
. D. FeCl
.
Câu 47: Cho hợp chất hữu cơ có công thức phân tử C
H
. Điều khẳng địmh nào sau đây là đúng ?
A. Phân tử C
H
có tổng số liên kết π và vòng bằng 2.
B. Phân tử C
H
là ankađien.
C. Phân tử C
H
có hai liên kết π
D. Phân tử C
H
là ankin.
Câu 48: Đốt cháy hoàn toàn m gam FeS
bằng một lượng O
vừa đủ, thu được khí X. Hấp thụ hết X vào 1 lít dung dịch chứa Ba(OH)
0,15 M và KOH 0,1 M, thu được dung dịch Y và 21,7 gam kết tủa. Cho Y vào dung dịch NaOH, thấy xuất hiện thêm kết tủa. Giá trị của m là
A. 12,6. B. 18,0. C. 24,0. D. 23,2.
Câu 49: Hỗn hợp A gồm FeS
và Cu
S. Hòa tan hoàn toàn A bằng dd HNO
đặc nóng, thu được 26,88 lít (đktc) khí X là sản phẩm khử duy nhất và dd B chỉ chứa 2 muối. Khối lượng của Cu
S trong hỗn hợp đầu là
A. 14,4 gam. B. 9,6 gam. C. 7,2 gam. D. 4,8 gam.
Câu 50: Có thể làm khô khí NH
bằng:
A. Khí HCl. B. P
O
. C. H
SO
đặc. D. CaO.
Đáp án đề thi thử THPT Quốc gia môn Hóa lần 2 năm 2016 – THPT Yên Lạc
| 352 | Đáp án | 352 | Đáp án | 352 | Đáp án | 352 | Đáp án | 352 | Đáp án |
| 1 | C | 11 | A | 21 | C | 31 | A | 41 | B |
| 2 | A | 12 | A | 22 | B | 32 | B | 42 | C |
| 3 | D | 13 | A | 23 | D | 33 | B | 43 | B |
| 4 | D | 14 | B | 24 | A | 34 | C | 44 | A |
| 5 | B | 15 | A | 25 | D | 35 | C | 45 | B |
| 6 | D | 16 | D | 26 | B | 36 | A | 46 | C |
| 7 | A | 17 | C | 27 | D | 37 | B | 47 | A |
| 8 | B | 18 | C | 28 | D | 38 | D | 48 | B |
| 9 | A | 19 | D | 29 | D | 39 | C | 49 | D |
| 10 | D | 20 | C | 30 | C | 40 | C | 50 | D |
Tất cả nội dung bài viết. Các em hãy xem thêm và tải file chi tiết tại đây:Download

