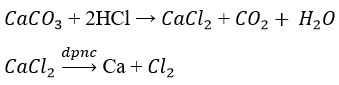
Bài 1 (trang 98 SGK Hóa 12): Trình bày các cách có thể :
– Điều chế Ca từ CaCO3
– Điều chế Cu từ CuSO4
Viết phương trình hóa học của các phản ứng
Lời giải:
Phương pháp để điều chế Ca là điện phân nóng chảy muối halogenua khan
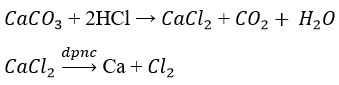
Từ CuSO4 điều chế Cu có thể dùng phương pháp : điện phân dung dịch , thủy luyện, nhiệt luyện.
– Thủy luyện : CuSO4 + Fe → FeSO4 + Cu
– Nhiệt luyện :
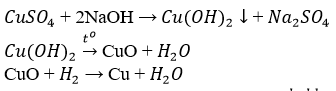
– Điện phân dung dịch :
![]()
Bài 2 (trang 98 SGK Hóa 12): Từ Cu(OH)2, MgO, Fe2O3 hãy điều chế các kim loại tương ứng bằng phương pháp thích hợp. Viết phương trình hóa học của phản ứng.
Lời giải:
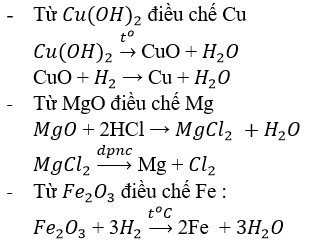
Bài 3 (trang 98 SGK Hóa 12): Một loại quặng sắt chứa 80% Fe2O3 và 10% SiO2. Hàm lượng các nguyên tử Fe và Si trong quặng này là :
A. 56% Fe và 4,7% Si
B. 54% Fe và 3,7% Si
C. 53% Fe và 2,7% Si
D. 52% Fe và 4,7% Si
Lời giải:
Giả sử có 100 gam quặng sắt, khối lượng Fe2O3 là 80 gam và khối lượng SiO2 là 10 gam
Số mol Fe2O3 là nFe2O3 = 80 / 160 = 0,5(mol)
nFe = 2 x nFe2O3 = 0,5.2 = 1(mol)
→ mFe = 1.56 = 56(g)
%mFe = 56 / 100 x 100% = 56%
Tương tự tính cho Si , %Si = 4,7%
Đáp án là A.
Bài 4 (trang 98 SGK Hóa 12): Để khử hoàn toàn 30 gam hỗn hợp gồm CuO, FeO, Fe3O4, Fe2O3,Fe, MgO cần dùng 5,6 lít khí CO (đktc). Khối lượng chất rắn thu được sau phản ứng là :
A. 28g.
B. 26g.
C. 24g.
D. 22g.
Lời giải:
Áp dụng định luật bảo toàn khối lượng ta có :
30 + mCO = m + mCO2 => m = 30 + 5,6 / 22,4 x 28 – 5,6/22,4 x 44 = 26 (g)
Đáp án B.
Bài 5 (trang 98 SGK Hóa 12): Điện phân (điện cực trơ) dung dịch muối sunfua của một kim loại hóa trị II với dòng điện cường độ 3A. Sau khi 1930 giây điện phân thấy khối lượng catot tăng 1,92 gam.
a. Viết phương trình hóa học của phản ứng xảy ra tại mỗi điện cực và phương trình hóa học chung của sự điện phân.
b. Xác định tên kim loại.
Lời giải:
