Đề thi thử THPT Quốc gia môn Hóa – THPT Yên Định 1, được tổ chức thi lần 1 năm 2016, các em tham khảo dưới đây:
Xem thêm: Đề thi thử THPT Quốc gia môn Hóa
|
SỞ GIÁO DỤC & ĐÀO TẠO THANH HÓA TRƯỜNG THPT YÊN ĐỊNH 1 (Đề thi gồm có 04 trang) |
ĐỀ KIỂM TRA KIẾN THỨC THI QUỐC GIA KHỐI 12 NĂM HỌC 2015-2016 LẦN 1 Môn: Hóa học Thời gian làm bài:90 phút; 50 câu trắc nghiệm |
|
ĐỀ CHÍNH THỨC |
Mã đề thi 132 |
(theo đvC) của các nguyên tố:
H = 1; C = 12; N = 14; O = 16; Na = 23; Mg = 24; Al = 27; S = 32; Cl = 35,5;
K = 39; Ca = 40; Ba = 137; Mn = 55; Fe = 56; Cu = 64; Zn = 65; Br = 80; Ag=108.
Câu 1: Đốt cháy hỗn hợp gồm 3 hiđrocacbon ta thu được 2,24 lít CO
(ở đktc) và 2,7 gam H
O. Thể tích khí O
đã tham gia phản ứng cháy (ở đktc) là
A. 3,92 lít. B. 5,6 lít. C. 4,48 lít. D. 2,8 lít.
Câu 2: Ở một loại polietilen có phân tử khối là 420000. Hệ số trùng hợp của loại polietien đó là
A. 15290 B. 17886 C. 12300 D. 15000
Câu 3: Khi thuỷ phân chất béo trong môi trường kiềm thì thu được muối của axit béo và chất nào trong số các chất sau?
A. Phenol. B. Este đơn chức. C. Glixerol. D. Ancol đơn chức.
Câu 4: Cho 1,17 gam một kim loại kiềm X tác dụng với nước (dư) thu được 0,336 lit khí H
(đktc). X là
A. Rb. B. Li. C. Na. D. K.
Câu 5: Cho các chất: glucozơ, saccarozơ, fructozơ, xenlulozơ, tinh bột. Số chất trong dãy tham gia phản ứng thủy phân là
A. 3. B. 1. C. 4. D. 2.
Câu 6: Tiến hành các thí nghiệm sau ở điều kiện thường:
(a) Sục khí vào dung dịch H
S (b) Sục khí F
vào nước
(c) Cho KMnO
vào dung dịch HCl đặc (d) Sục khí CO
vào dung dịch NaOH
(e) Cho Si vào dung dịch NaOH (g) Cho Na
SO
vào dung dịch H
SO
Số thí nghiệm có sinh ra đơn chất là
A. 4. B. 3. C. 5. D. 6.
Câu 7: Este X có công thức cấu tạo thu gọn là CH
COOCH
. Tên gọi của X là
A. etyl fomat. B. metyl axetat. C. metyl fomat. D. etyl axetat.
Câu 8: Khi cho brom lỏng vào ống nghiệm chứa benzen, lắc kĩ rồi để yên. Hiện tượng quan sát được là:
A. màu brom đậm dần.
B. có khí thoát ra, màu brom nhạt đi.
C. tạo thành một thể đồng nhất có màu nhạt hơn brom lỏng.
D. chất lỏng phân thành 2 lớp, lớp trên màu vàng, lớp dưới không màu.
Câu 9: Tơ lapsan thuộc loại tơ
A. thiên nhiên. B. poliamit. C. Polieste. D. nhân tạo.
Câu 10: Cho các cân bằng sau:
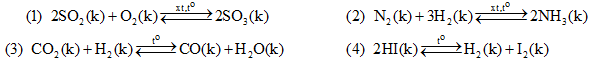
Khi thay đổi áp suất, nhóm gồm các cân bằng hoá học đều không bị chuyển dịch là
A. (1) và (3). B. (3) và (4). C. (2) và (4). D. (1) và (2).
Câu 11: Anilin (C
H
NH
) và phenol (C
H
OH) đều phản ứng với
A. nước Br
. B. dd NaOH. C. dd HCl. D. dd NaCl.
Câu 12: Kim loại nào sau đây tác dụng với Cl
và HCl tạo ra cùng một muối là
A. Cu. B. Mg. C. Fe. D. Ag.
Câu 13: Hòa tan hoàn toàn 5,6 gam Fe trong dung dịch HNO
loãng, dư, sinh ra V lít khí NO (sản phẩm khử duy nhất, đktc). Giá trị V là
A. 6,72. B. 3,36. C. 2,24. D. 4,48.
Câu 14: Một dung dịch chứa 0,2 mol Na
; 0,1 mol Mg
; 0,05 mol Ca
; 0,15 mol và x mol Cl
. Giá trị của x là
A. 0.35. B. 0,3. C. 0,15. D. 0,20.
Câu 15: Khi điện phân nóng chảy NaCl (điện cực trơ), tại catôt xảy ra
A. sự oxi hoá ion Cl
. B. sự oxi hoá ion Na
.
C. sự khử ion Cl
. D. sự khử ion Na
.
Câu 16: Để khử mùi tanh của cá (gây ra do một số amin) ta có thể rửa cá với chất nào trong các chất sau?
A. Nước muối .B. Giấm. C. Nước cất. D. Nước vôi trong.
Câu 17: Trong số các kim loại sau: Ag, Cu, Au, Al. Kim loại có độ dẫn điện tốt nhất ở điều kiện thường là
A. Al. B. Au. C. Cu. D. Ag.
Câu 18: Thuỷ phân các chất sau trong môi trường kiềm:
(1) CH
Cl-CH
Cl;
(2) CH
-COO-CH=CH
; (3) CH
– COO-CH
-CH=CH
; (4) CH
-CH
-CHCl
; (5) CH
-COO-CH
Cl Các chất phản ứng tạo sản phẩm có phản ứng tráng bạc là:
A. (2), (3), (4). B. (1) ,(2) ,(4). C. (1) , (2), (3). D. (2), (4),(5).
Câu 19: Ba hợp chất hữu cơ X, Y, Z có cùng công thức phân tử C
H
O
. X và Y đều tham gia phản ứng tráng bạc; X, Z có phản ứng cộng hợp Br
; Z tác dụng với NaHCO
. Công thức cấu tạo của X, Y, Z lần lượt là
A. OHC-CH
-CHO; HCOOCH=CH
, CH
=CH-COOH.
B. CH
-CO-CHO; HCOOCH=CH
, CH
=CH-COOH.
C. HCOOCH=CH
; OHC-CH
-CHO, CH
=CH-COOH.
D. HCOOCH=CH
; CH
=CH-COOH, HCO-CH
-CHO.
Câu 20: Một nguyên tử của nguyên tố X có tổng số hạt proton, nơtron, electron là 52 và có số khối là 35. Số hiệu nguyên tử của nguyên tố X là
A. 18. B. 17. C. 15. D. 23.
Câu 21: Hòa tan hỗn hợp hai khí: CO
và NO
vào dung dịch KOH dư, thu được hỗn hợp các muối là
A. KHCO
, KNO
. B. K
CO
, KNO
, KNO
.
C. KHCO
, KNO
, KNO
. D. K
CO
, KNO
.
Câu 22: Cho 10,8 gam kim loại M tác dụng hoàn toàn với khí Cl
dư thu được 53,4 gam muối clorua. Kim loại M là
A. Mg. B. Al. C. Fe. D. Zn.
Câu 23: Khi cho luồng khí hidro(dư) đi qua ống nghiệm chứa Al
O
, FeO, CuO, MgO nung nóng, đến khi phản ứng xảy ra hoàn toàn. Chất rắn còn lại trong ống nghiệm là:
A. Al, Fe, Cu, Mg. B. Al
O
, FeO, CuO, MgO.
C. Al
O
, Fe, Cu, MgO. D. Al, Fe, Cu, MgO.
Câu 24: Dãy gồm các chất mà trong phân tử chỉ có liên kết cộng hoá trị phân cực là:
A. HCl, O
, H
S B. H
O, HF, NH
. C. HF, Cl
, H
O D. O
, H
O, NH
Câu 25: Đốt cháy hoàn toàn m gam hỗn hợp gồm C
H
, C
H
, C
H
thu được 1,68 lít khí CO
(đktc). Giá trị của m là
A. 0,95. B. 1,15. C. 1,05. D. 1,25.
Câu 26: Một oxit kim loại có phần trăm theo khối lượng của oxi trong oxit là 20%. Công thức của oxit là
A. CuO. B. FeO. C. MgO. D. Na
O.
Câu 27: Xà phòng hóa 8,8 gam CH
COOC
H
bằng dung dịch NaOH vừa đủ. Sau khi phản ứng xảy ra hoàn toàn, cô cạn dung dịch thu được chất rắn khan có khối lượng là
A. 3,28 gam. B. 10,4 gam. C. 8,56 gam. D. 8,2 gam.
Câu 28: Cho các hợp chất hữu cơ:
(1) ankan; (2) ancol no, đơn chức, mạch hở;
(3) Monoxicloankan; (4) ete no, đơn chức, mạch hở;
(5) anken; (6) ancol không no (có một liên kết đôi C=C), mạch hở
(7) ankin; (8) anđehit no, đơn chức, mạch hở;
(9) axit no, đơn chức, mạch hở (10) axit không no (có một liên kết đôi C=C), đơn chức.
Dãy gồm các chất khi đốt cháy hoàn toàn đều cho số mol CO
bằng số mol H
O là
A. (3), (5), (6), (8), (9). B. (3), (4), (6), (7), (10).
C. (2), (3), (5), (7), (9). D. (1), (3), (5), (6), (8).
Câu 29: Dãy gồm các ion có thể cùng tồn tại trong 1 dung dịch là
A. Ca
, Cl
, Na
, CO
. B. K
, Ba
, OH
, Cl
.
C. Al
, SO
, Cl
, Ba
. D. Na
, OH
, HCO
, K
.
Câu 30: Số nguyên tố mà nguyên tử của nó ở trạng thái cơ bản có phân lớp electron lớp ngoài cùng 4s1 là
A. 3. B. 1. C. 2. D. 4.
Câu 31: Đun nóng 18 gam glucozơ với dung dịch AgNO
/NH
dư thì thu được m gam Ag. Giá trị của m là
A. 2,16. B. 10,8. C. 21,6. D. 7,20.
Câu 32: Trong các chất: m-HOC
H
OH; p-CH
COOC
H
OH; CH
CH
COOH;
(CH
NH
)
CO
; CH
(Cl)COOC
H
; HOOCCH
CH(NH
)COOH; ClH
NCH(CH
)COOH
Số chất mà 1 mol chất đó phản ứng được tối đa với 2 mol NaOH là
A. 4. . B. 3. C. 6. D. 5.
Câu 33: Cho sơ đồ phản ứng sau:
C
H
→ C
H
→ C
H
Cl → C
H
OH → CH
CHO → CH
COOH → CH
COOC
H
Số phản ứng trong sơ đồ chuyển hoá trên thuộc phản ứng oxi hoá khử là
A. 3. B. 5. C. 6. D. 4.
Câu 34: Trong phương trình phản ứng:
aK
SO
+ bKMnO
+ cKHSO
→ dK
SO
+ eMnSO
+ gH
O.
Tổng hệ số tối giản các chất tham gia phản ứng là
A. 15. B. 18. C. 10. D. 13.
Câu 35: Cho 28 gam hỗn hợp X gồm CO
và SO
( = 1,75) lội chậm qua 500 ml dung dịch chứa hỗn hợp NaOH 0,7M và Ba(OH)
0,4M được m gam kết tủa. Giá trị của m là
A. 52,25. B. 49,25. C. 41,80. D. 54,25.
Câu 36: Cho 28,1g hỗn hợp gồm Fe
O
, MgO, ZnO tác dụng vừa đủ với 250 ml dd H
SO
2M. Cô cạn dung dịch thu được khối lượng muối khan là
A. 68,1 gam. B. 61,4 gam. C. 48,1 gam. D. 77,1 gam.
Câu 37: Cho 17,9 gam hỗn hợp Fe, Cu và Al vào bình đưng 200 gam dung dịch H
SO
24,01%. Sau khi các phản ứng xảy ra hoàn toàn thu được 9,6 gam chất rắn và có 5,6 lit khí đktc thoát ra. Thêm tiếp vào bình 10,2 gam NaNO
, khi các phản ứng kết thúc thì thể tích khí NO (đktc, sản phẩm khử duy nhất) tạo thành và khối lượng muối thu được sau khi cô cạn dung dịch là
A. 2,688 và 64,94. B. 2,688 và 67,7. C. 2,24 và 56,3. D. 2,24 và 59,18.
Câu 38: Hỗn hợp X gồm CuSO
, Fe
(SO
)
, MgSO
, trong X oxi chiếm 47,76% khối lượng. Hòa tan hết 26,8 gam hỗn hợp X vào nước được dung dịch Y, cho dung dịch Ba(OH)
dư vào dung dịch Y thấy xuất hiện m gam kết tủa. Giá trị của m gần nhất với giá trị nào sau đây:
A. 46,6. B. 61,0. C. 55,9. D. 57,6.
Câu 39: Cho m gam bột Cu vào 400 ml dung dịch AgNO
0,2M, sau một thời gian phản ứng thu được 7 gam hỗn hợp chất rắn X và dung dịch Y. Lọc tách X, rồi thêm 3,9 gam bột Zn vào dung dịch Y, sau khi phản ứng xảy ra hoàn toàn thu được 6,14 gam chất rắn. Giá trị của m là
A. 5,76. B. 6,40. C. 3,20. D. 3,84.
Câu 40: Cho hỗn hợp gồm 0,1 mol HCHO và 0,1 mol HCOOH tác dụng với dung dịch AgNO
/ NH
dư, đun nóng. Sau khi các phản ứng xảy ra hoàn toàn, khối lượng Ag tạo thành là
A. 10,8 gam. B. 21,6 gam. C. 43,2 gam. D. 64,8 gam.
Câu 41: Đốt cháy hoàn toàn 0,1 mol một peptit X (X được tạo thành từ các amino axit chỉ chứa 1 nhóm -NH
và 1 nhóm -COOH) cần 58,8 lít O
thu được 49,28 lit CO
và 33,3 gam H
O (Các thể tích khí đo đktc). Nếu cho 0,1 mol X trên thủy phân hoàn toàn trong 500 ml dung dịch NaOH 2M thu được dung dịch Y, cô cạn Y thu được m gam chất rắn. Số liên kết peptit trong X và giá trị của m lần lượt là
A. 9 và 92,9 gam. B. 8 và 96,9 gam. C. 10 và 96,9 gam. D. 10 và 92,9 gam.
Câu 42: Cho 0,1 mol axit axetic vào cốc chứa 30 ml dung dịch MOH 20% (D = 1,2 g/ml, M là kim loại kiềm). Cô cạn dung dịch sau phản ứng, thu được m gam chất rắn khan. Đốt cháy hoàn toàn chất rắn thu được 9,54 gam M
CO
và hỗn hợp khí, dẫn hỗn hợp qua dung dịch nước vôi trong dư thì khối lượng dung dịch thay đổi như thế nào?
A. Giảm 5,70 gam. B. Tăng 5,70 gam. C. Giảm 2,74 gam. D. Tăng 2,74 gam.
Câu 43: Hỗn hợp R chứa các hợp chất hữu cơ đơn chức gồm axit (X), ancol (Y) và este (Z) (được tạo thành từ X và Y). Đốt cháy hoàn toàn 2,15 gam este (Z) trong O
vừa đủ rồi hấp thụ sản phẩm cháy vào dung dịch Ba(OH)2 dư được 19,7 gam kết tủa và khối lượng dung dịch giảm 13,95 gam. Mặt khác, 2,15 gam Z tác dụng vừa đủ với NaOH được 1,7 gam muối. Axit X và ancol Y tương ứng là
A. HCOOH và C
H
OH. B. C
H
COOH và CH
OH.
C. HCOOH và C
H
OH. D. CH
COOH và C
H
OH.
Câu 44: X là hỗn hợp gồm propan, xiclopropan, butan và xiclobutan. Đốt cháy hoàn toàn m gam hỗn hợp X thu được 63,8 gam CO
và 28,8 gam H
O. Thêm H
vừa đủ vào m gam X rồi đun nóng với Ni thu được hỗn hợp Y có tỉ khối so với H
là 26,375. Tỉ khối của X so với H
là:
A. 22,89. B. 24,52. C. 23,95. D. 25,75.
Câu 45: Điện phân (với điện cực trơ) dung dịch NaOH a% với cường độ dòng điện 19,3A, sau 60 phút thu được 100 gam dung dịch X có nồng độ 24%. Giá trị a là
A. 22,54. B. 24. C. 25,66. D. 21,246.
Câu 46: Hỗn hợp M gồm 2 andehit đơn chức, mạch hở X và Y (phân tử Y nhiều hơn phân tử X một liên kết ).Hidro hóa hoàn toàn 10,1 gam M cần dùng 7,84 lit khí H
vừa đủ (đktc) thu được hỗn hợp N gồm 2 ancol tương ứng. Cho toàn bộ lượng N phản ứng hết với 6,9 gam Natri. Sau các phản ứng xảy ra hoàn toàn thu được17,45 gam chất rắn. Công thức của X, Y lần lượt là:
A. CH
CHO và C
H
CHO. B. CH
CHO và C
H
CHO.
C. HCHO và C
H
CHO. D. HCHO và C
H
CHO.
Câu 47: Hòa tan 54,44 gam hỗn hợp X gồm PCl
và PBr
vào nước được dung dịch Y. Để trung hòa hoàn toàn dung dịch Y cần 500 ml dung dịch KOH 2,6M. % khối lượng của PCl
trong X gần nhất với giá trị nào sau đây:
A. 26,96%. B. 12,125. C. 8,08%. D. 30,31%.
Câu 48: Cho 0,01 mol aminoaxit X phản ứng vừa đủ với 0,02 mol HCl hoặc 0,01 mol NaOH. Công thức của X có dạng nào trong các dạng sau?
A. H
NR(COOH)
. B. (H
N)
R(COOH)
. C. H
NRCOOH. D. (H
N)
RCOOH.
Câu 49: Nung nóng m gam hỗn hợp gồm Al và Fe
O
trong điều kiện không có không khí. Sau khi các phản ứng xảy ra hoàn toàn thu được hỗn hợp rắn X. Cho X tác dụng với dung dịch NaOH dư thu được dung dịch Y, chất rắn Z và có 3,36 lit khí H
đktc. Sục khí CO
dư vào dung dịch Y thu được 39 gam kết tủa. Giá trị của m là
A. 36,7. B. 45,6. C. 48,3. D. 57,0.
Câu 50: Hỗn hợp khí X gồm đimetylamin và hai hiđrocacbon đồng đẳng liên tiếp. Đốt cháy hoàn toàn 100 ml hỗn hợp X bằng một lượng oxi vừa đủ, thu được 550 ml hỗn hợp Y gồm khí và hơi nước. Nếu cho Y đi qua dung dịch axit sunfuric đặc (dư) thì còn lại 250 ml khí (các thể tích khí và hơi đo ở cùng điều kiện). Công thức phân tử của hai hiđrocacbon là
A. C
H
và C
H
. B. C
H
và C
H
. C. CH
và C
H
. D. C
H
và C
H
.
Theo Tuyensinh247.com
Tất cả nội dung bài viết. Các em hãy xem thêm và tải file chi tiết tại đây:Download