Đáp án đề thi thử THPT Quốc gia môn Hóa năm 2016 đề số 5, đây là dề thi giúp các em làm quen với các dạng bài có trong kì thi này
Xem thêm: Đề thi thử THPT Quốc gia môn Hóa
Cho: H = 1; C = 12; N = 14; O = 16; F = 19; Na = 23; Mg = 24; Al = 27; Si = 28; P = 31; S = 32; Cl = 35,5; K = 39; Ca = 40; Fe = 56; Ba = 137; Zn = 65; Cu = 64.
Câu 1:Trong các cặp chất cho dưới đây, cặp chất nào có thể cùng tồn tại trong một dung dịch ?
A.NaCl và AgNO
. B.NaAlO
và HCl.
C.NaHSO
và NaHCO
. D.AlCl
và CuSO
.
Câu 2:Hỗn hợp X gồm axetilen (0,15 mol), vinylaxetilen (0,1 mol), etilen ( 0,1 mol) và hiđro (0,4 mol). Nung X với xúc tác niken một thời gian thu được hỗn hợp Y có tỉ khối đối với hiđro bằng 12,7. Hỗn hợp Y phản ứng vừa đủ với dung dịch chứa a mol Br
. Giá trị của a là
A.0,45. B.0,25. C.0,65. D.0,35.
Câu 3:Dãy các chất được xếp theo chiều tăng dần tính axit là:
A.HClO
<HClO
<HClO
B. HClO
<HClO
<HClO
<HClO
C.HClO< HClO
< HClO
< HClO
D.HClO
<HClO
2
Câu 4:Cho hình vẽ mô tả thí nghiệm điều chế khí Y từ dung dịch X:
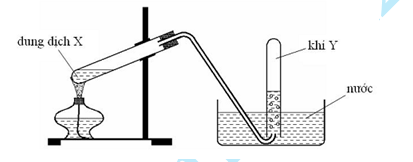
Hình vẽ trên minh họa phản ứng nào sau đây?
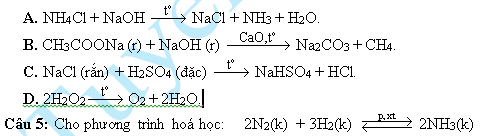
Nếu ở trạng thái cân bằng nồng độ của NH
là 0,30mol/l, của N
là 0,05mol/l và của H
là 0,10mol/l. Hằng số cân bằng của hệ là giá trị nào sau đây?
A.3600. B.360000. C.36000. D.360.
Câu 6:Số liên kết peptit trong hợp chất sau là
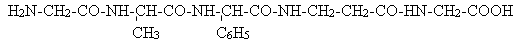
A.3. B.2. C.4. D.1.
Câu 7:Cho khí CO dư qua hỗn hợp nung nóng gồm Al
O
,CuO, Fe
O
, MgO. Chất rắn sau phản ứng thu được là
A.Al
O
, Cu, Fe, Mg B.Al, Cu, Fe, MgO C.Al, Cu, Fe, Mg D.Al
O
, Cu, Fe, MgO
Câu 8:Moät dung dòch coù chöùa 2 cation Fe
(0,1 mol) Al
(0,2 mol) vaø 2 anion Cl
(x mol) vaø SO
(y mol). Khi coâ caïn dung dòch thu ñöôïc 46,9 gam muoái khan .Tìm x vaø y
A.0,1 vaø 0,2 mol B.0,3 vaø 0,2 mol C.0,2 vaø 0,3 mol D.0,2 vaø 0,4 mol
Câu 9:Khi cho từ từ dung dịch NH
vào dung dịch CuSO
cho đến dư thì
A.sau một thời gian mới thấy kết tủa xuất hiện. B.không thấy kết tủa xuất hiện.
C.có kết tủa xanh xuất hiện sau đó tan ra. D.có kết tủa xanh xuất hiện và không tan.
Câu 10:Theo Bronstet ion nào sau đây là lưỡng tính?
1. PO
2. CO
3. HSO
4. HCO
5. HPO
A.3, 4, 5. B.1, 2, 5. C.2, 4, 5. D.1, 4, 5.
Câu 11:Lấy m gam Kali cho tác dụng 500 ml dung dịch HNO
thu được dung dịch M và thoát ra 0,336 lít hỗn hợp X (đkc) gồm 2 khí A & B. Cho thêm vào dd M dung dịch KOH dư thì thấy thoát ra 0,224 lít khí B. Biết rằng quá trình khử HNO
chỉ tạo một sản phẩm duy nhất. Xác định m:
A.7,8g B.12,48g C.3,12g D.6,63g
Câu 12:Hỗn hợp rắn X gồm Fe, FeO, Fe
O
, Fe
O
với số mol mỗi chất là 0,1 mol. Hòa tan hết X vào dd Y gồm HCl và H
SO
loãng dư thu được dd Z. Nhỏ từ từ dd Cu(NO
)
1M vào dd Z cho tới khi khí NO ngừng thoát ra. Thể tích dung dịch Cu(NO
)
cần dùng và thể tích khí thoát ra ở đktc là
A.500ml; 2,24lit B.50ml; 1,12lit C.50ml; 2,24lit D.25 ml; 1,12lit
Câu 13:Một hỗn hợp gồm 2 ankin khi đốt cháy cho ra 13,2 gam CO
và 3,6 gam H
O. Tính khối lượng brom có thể cộng vào hỗn hợp trên
A.32 gam. B.4 gam. C.24 gam. D.16 gam.
Câu 14:Có các ion kim loại: Zn
, Sn
, Ni
, Fe
, Pb
. Thứ tự tính oxi hóa của các ion kim loại giảm dần là
A.Pb
> Sn
> Fe
> Ni
> Zn
B.Sn
> Ni
> Zn
> Pb
> Fe
C.Pb
> Sn
> Ni
> Fe
> Zn
D.Zn
> Sn
> Ni
> Fe
> Pb
Câu 15:Cho 0,02 mol a-amino axit X tác dụng vừa đủ với dd chứa 0,04 mol NaOH. Mặt khác 0,02 mol X tác dụng vừa đủ với dd chứa 0,02 mol HCl, thu được 3,67 gam muối. Công thức của X là
A.HOOC-CH2CH2CH(NH2)-COOH. B.CH3CH(NH2)-COOH.
C.H2N-CH2CH(NH2)-COOH. D.HOOC-CH2CH(NH2)-COOH.
Câu 16:Dãy gồm các chấtđược xếp theo chiều nhiệtđộsôi tăng dần từtrái sang phải là:
A.CH
COOH, C
H
, CH
CHO, C
H
OH. B.C
H
, CH
CHO, C
H
OH, CH
COOH.
C.C
H
, C
H
OH, CH
CHO, CH
COOH. D.CH
CHO, C
H
OH, C
H
, CH
COOH.
Câu 17:Dãy chất nào sau đây, trong nước đều là chất điện li yếu ?
A.H
CO
, H
SO
, HClO, Al
(SO
)
. B.H
S, CH
COOH, HClO, NH
.
C.H
CO
, H
PO
, CH
COOH, Ba(OH)
. D.H
S, H
SO
, H
SO
, NH
.
Câu 18:Cho sơ đồ phản ứng sau:
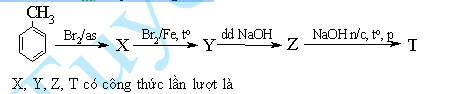
A.p-CH
C
H
Br, p-CH
BrC
H
Br, p-HOCH
C
H
Br, p-HOCH
C
H
ONa.
B.p-CH
C
H
Br, p-CH
BrC
H
Br, p-CH
BrC
H
OH, p-CH
OHC
H
ONa.
C.CH
Br-C
H
, p-CH
Br-C
H
Br, p-CH
C
H
OH, p-CH
OHC
H
ONa.
D.CH
BrC
H
, p-CH
Br-C
H
Br, p-HOCH
C
H
Br, p-HOCH
C
H
ONa.
Câu 19:Hỗn hợp X có tỷ khối so với H
là 21,2 gồm propan, propen và propin. Khi đốt cháy hoàn toàn 0,1 mol X, tổng khối lượng của CO
và H
O thu được là:
A.18,96 gam B.16,80 gam C.20,40 gam D.18,60 gam
Câu 20:X, Y, Z là 3 ancol liên tiếp trong dãy đồng đẳng, trong đó M
= 1,875M
. X có đặc điểm là
A.Hòa tan được Cu(OH)
.
B.Tách nước tạo 1 anken duy nhất.
C.Không có đồng phân cùng chức hoặc khác chức.
D.Chứa 1 liên kết trong phân tử.
Câu 21:Cho phản ứng: Al + OH
+ NO
+ H
O → AlO
+ NH
↑
Tổng hệ số cân bằng ( hệ số cân bằng là các số nguyên tối giản) của phản ứng trên bằng
A.22 B.38 C.29 D.30
Câu 22:Cho các hợp chất hữu cơ thuộc các dãy đồng đẳng sau:
(1) ankan;
(2) ancol no, đơn chức, mạch hở;
(3) monoxicloankan;
(4) ete no, đơn chức, mạch hở;
(5) anken;
(6) ancol không no (có một liên kết đôi C=C), mạch hở;
(7) ankin;
(8) anđehit no, đơn chức, mạch hở;
(9) axit no, đơn chức, mạch hở;
(10) axit không no (có một liên kết đôi C=C), đơn chức;
(11) este no, đơn chức, mạch hở;
(12) glucozo dạng mạch hở; frutozo dạng mạch hở;
Số dãy đồng đẳng mà khi đốt cháy hoàn toàn đều cho số mol CO
bằng số mol H
O là
A.7. B.5. C.6. D.8.
Câu 23:Hòa tan hoàn toàn 5,18 gam hỗn hợp gồm Al
O
, Fe
O
, CuO, ZnO trong 500 ml axit H
SO
0,1M (vừa đủ). Sau phản ứng, hỗn hợp muối sunfat khan thu được khi cô cạn dung dịch có khối lượng là
A.9,18 gam. B.7,18 gam. C.11,18 gam. D.8,18 gam.
Câu 24:Dung dịch X gồm 0,1 mol K+; 0,2 mol Mg2+; 0,1 mol Na+; 0,2 mol Cl- và a mol Y
. Cô cạn dung dịch X, thu được m gam muối khan. Ion Y
phù hợp và giá trị của m là
A.CO
và 30,1. B.CO
và 42,1. C.SO
và 56,5. D.SO
và 37,3.
Câu 25:Cho các cân bằng sau:
(1) 2NH
⇌ N
+ 3H
H > 0 (3) CaCO
⇌ CaO
+ CO
H > 0
(2) 2SO
+ O
⇌ 2SO
H < 0 (4) H
+ I
⇌ 2HI
H < 0
Trong các cân bằng trên cân bằng nào sẽ chuyển dịch theo chiều thuận khi tăng nhiệt độ và giảm áp suất?
A.1, 3. B.1, 4. C.1, 2, 3 ,4. D.2, 4.
Câu 26:Khi nhỏ từ từ dung dịch chứa x mol NaOH vào dung dịch hỗn hợp gồm 0,8 mol HCl và 0,6 mol AlCl3, kết quả thí nghiệm được biểu diễn trên đồ thị sau:
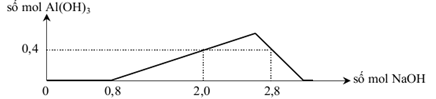
Tính khối lượng kết tủa thu được tại thời điểm số mol NaOH tiêu tốn là 2,7 mol
A.35,1 gam. B.39 gam. C.46,8 gam. D.23,4 gam.
Câu 27: Đun 12 gam axit axetic với 13,8 gam etanol (có H
SO
đặc làm xúc tác) đến khi phản ứng đạt tới trạng thái cân bằng thu được 11 gam este. Hiệu suất của phản ứng este hoá là
A.55%. B.75%. C.50%. D.62,5%.
Câu 28:X là hợp chất có công thức phân tử C
H
O
. X tác dụng với Na dư cho số mol H
bay ra bằng số mol NaOH cần dùng để trung hòa cũng lượng X trên. Chỉ ra công thức cấu tạo thu gọn của X.
A.C
H
COOH. B.HOC
H
CH
OH. C.CH
OC
H
OH. D.CH
C
H
(OH)
.
Câu 29:Cho 0,1 mol mỗi chất gồm: Zn, Fe, Cu tác dụng hết với dung dịch HNO
dư thu được dung dịch X và 2,688 lít hỗn hợp gồm NO
, NO, N
O, N
. Trong đó số mol NO
bằng số mol N
. Cô cạn dung dịch X thu được 58,8 gam muối. Số mol HNO
tham gia phản ứng là
A.0,868 . B.0,893. C.0,832. D.0,845.
Câu 30:Nung nóng 19 gam hỗn hợp Fe, Al, Zn, Mg với một lượng dư khí O
, đến khi các phản ứng xảy ra hoàn toàn, thu được 27 gam chất rắn X. Thể tích dung dịch H
SO
1M vừa đủ để phản ứng với chất rắn X là
A.800 ml. B.200 ml. C.500 ml. D.400 ml.
Câu 31:Hỗn hợp chất rắn X gồm 0,2 mol FeO; 0,2 mol Fe
O
và 0,1 mol Fe
O
. Hòa tan hoàn toàn hỗn hợp X trong HCl dư thu được dung dịch Y. Cho dung dịch Y tác dụng với dung dịch NaOH dư, thu được dung dịch T và kết tủa Z. Lọc kết tủa Z nung trong không khí đến khối lượng không đổi thu được chất rắn E có khối lượng là:
A.80 gam B.64 gam C.52 gam D.72 gam
Câu 32:Hòa tan 14 gam hỗn hợp Cu, Fe
O
vào dung dịch HCl, sau phản ứng còn dư 2,16 gam hỗn hợp chất rắn và dung dịch X. Cho X tác dụng với dung dịch AgNO
dư thì thu được bao nhiêu gam kết tủa? Biết các phản ứng xảy ra hoàn toàn.
A.12,96. B.47,42. C.45,92. D.58,88.
Câu 33:Phát biểu nào sauđây làđúng?
C.Amilopectin có cấu trúc mạch phân nhánh. D.Glucozơ bị khử bởi dd AgNO
trong NH
.
Câu 34:Trong các phản ứng sau, phản ứng nào HCl đóng vai trò là chất oxi hoá?
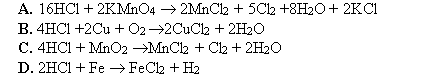
Câu 35:Cho 15,2 gam hỗn hợp chất hữu cơ A phản ứng vừa đủ với 300 ml dung dịch NaOH 1M thu được dung dịch B. Cô cạn dung dịch B chỉ thu được hơi nước 23,6 gam hỗn hợp muối khan C. Đốt cháy hoàn toàn C thu được Na
CO
, 14,56 lít CO
(đkc) và 6,3 gam H
O. (Biết CTPT của A trùng với CTĐGN). Xác định số đồng phân có thể có của
A.10 B.9 C.7 D.8
Câu 36:Cho m gam hỗn hợp X gồm hai rượu (ancol) no, đơn chức, kế tiếp nhau trong dãy đồng đẳng tác dụng với CuO dư, nung nóng, thu được một hỗn hợp rắn Z và một hỗn hợp hơi Y (có tỷ khối hơi so với H
là 13,75). Cho toàn bộ Y phản ứng với một lượng dư Ag
O (hoặc AgNO
) trong dung dịch NH
nung nóng, sinh ra 64,8 gam Ag. Giá trị của m là:
A.7,4 B.7,8 C.8,8 D.9,2
Câu 37:Trong số các chất sau:HNO
, CH
COOH,KMnO
, C
H
,HCOOH, HCOOCH
, C
H
O
, C
H
OH, SO
, Cl
, NaClO, CH
, NaOH, NH
H
S. Số chất thuộc loại chất điện li là
A.7. B.8. C.9. D.10.
Câu 38:Hoà tan 6,0 gam hỗn hợp X gồm Mg, Al, Zn trong dung dịch HNO
vừa đủ, sau phản ứng hoàn toàn thu được dung dịch Y và hỗn hợp gồm 0,02 mol NO và 0,02 mol N
O. Làm bay hơi dung dịch Y thu được 25,4 gam muối khan. Số mol HNO
bị khử trong phản ứng trên là
A.0,09 mol B.0,06 mol C.0,08 mol D.0,07 mol
Câu 39:Một cốc dung dịch chứa các ion: a mol Na
, b mol Al
, c mol SO
, d mol Cl
. Biểu thức liên hệ a,b,c,d, là
A.a + 3b = c + d B.a + 3b = 2c + d C.a +2b = c +d D.a +2b = c + 2d
Câu 40:Cho một dòng điện có cường độ I không đổi đi qua 2 bình điện phân mắc nối tiếp, bình 1 chứa 100ml dung dịch CuSO
0,01M, bình 2 chứa 100 ml dung dịch AgNO
0,01M. Biết rằng sau thời gian điện phân 500 giây thì bên bình 2 xuất hiện khí ở catot, tính cường độ I và khối lượng Cu bám bên catot của bình 1 và thể tích khí(đktc) xuất hiện bên anot của bình 1.
A.0,386A; 0,64g Cu; 22,4 ml O
B.0,193A; 0,032g Cu; 22,4 ml O
C.0,193A; 0,032g Cu; 5,6 ml O
D.0,193A; 0,032g Cu; 11,2 ml O
Câu 41:Tiến hành các thí nghiệm sau:
(1) Sục khí NH
tới dư vào dung dịch CuSO
(2) Sục khí etilen vào dung dịch KMnO
.
(3) Sục khí H
S vào dung dịch FeCl
.
(4) Cho dung dịch NaOH tới dư vào dung dịch AlCl
.
(5) Sục khí CO
tới dư vào dung dịch NaAlO
(hoặc Na[Al(OH)
]).
(6) Cho dung dịch HCl tới dư vào dung dịch NaAlO
(hoặc Na[Al(OH)
]).
(7) Sục khí NH
tới dư vào dung dịch Al
(SO
)
.
(8) Cho dung dịch NaOH tới dư vào dung dịch Ca(HCO
)
.
(9) Sục khí C
H
vào dung dịch AgNO
trong môi trường NH
.
(10) Sục khí H
S vào dung dịch CuSO
;
Sau khi các phản ứng kết thúc, có bao nhiêu thí nghiệm thu được kết tủa?
A.6. B.5. C.4. D.7.
Câu 42:Sự tách hiđro halogenua của dẫn xuất halogen X có CTPT C
H
Cl cho 2 olefin đồng phân, X là chất nào trong những chất sau đây ?
A.iso-butyl clorua. B.sec-butyl clorua. C.tert-butyl clorua. D.n- butyl clorua.
Câu 43:Cho phản ứng thuận nghịch:

Ở t
C có hằng số cân bằng K
= 2,25. Cần lấy bao nhiêu mol CH
COOH trộn với 1 mol C
H
OH để hiệu suất phản ứng đạt 70% (tính theo C
H
OH) ở t
C?
A.1,000 mol. B.1,426 mol. C.1,500 mol. D.2,925 mol.
Câu 44:Hỗn hợp X gồm axit panmitic, axit stearic và axit linoleic. Để trung hoà m gam X cần 40 ml dung dịch NaOH 1M. Mặt khác, nếu đốt cháy hoàn toàn m gam X thì thu được 15,232 lít khí CO
(đktc) và 11,7 gam H
O. Số mol của axit linoleic trong m gam hỗn hợp X là
A.0,010. B.0,005. C.0,020. D.0,015.
Câu 45:Hòa tan hết m gam hỗn hợp Fe, Zn bằng dung dịch H
SO
10% vừa đủ, thu được dung dịch có nồng độ phần trăm của muối sắt là 4,87%. Nồng độ phần trăm của muối kẽm trong dung dịch là:
A.10,32% B.8,72% C.10,95% D.10,30%
Câu 46:Đun nóng 13,875 gam một ankyl clorua Y với dung dịch NaOH, tách bỏ lớp hữu cơ, axit hóa phần còn lại bằng dung dịch HNO
, nhỏ tiếp vào dung dịch AgNO
dư thấy tạo thành 21,525 gam kết tủa. Chất Y có bao nhiêu đồng phân dẫn xuất halogen bậc 2.
A.4. B.1. C.3. D.2.
Câu 47:Hòa tan hoàn toàn 17,88g hỗn hợp gồm 2 kim loại kiềm A, B và kim loại kiềm thổ M vào nước thu được dd Y và 0,24 mol khí H
. Dung dịch Z gồm H
SO
và HCl, trong đó số mol HCl gấp 4 lần số mol H
SO
. Để trung hòa ½ dd Y cần hết V lit dd Z. Tổng khối lượng muối khan tạo thành trong phản ứng trung hòa là
A.24,7g B.18,64g C.27,4g D.18,46g
Câu 48:Gluxit (cacbohiđrat) chỉchứa hai gốc glucozơtrong phân tửlà
A.xenlulozơ. B.tinh bột. C.mantozơ. D.saccarozơ.
Câu 49:Cho hỗn hợp X gồm CH
, C
H
và C
H
. Lấy 8,6 gam X tác dụng hết với dung dịch brom (dư) thì khối lượng brom phản ứng là 48 gam. Mặt khác, nếu cho 13,44 lít (ở đktc) hỗn hợp khí X tác dụng với lượng dư dung dịch AgNO
trong NH
, thu được 36 gam kết tủa. Phần trăm thể tích của CH
có trong X là
A.50%. B.40%. C.20%. D.25%.
Câu 50:Đốt cháy hoàn toàn 0,4 mol hỗn hợp X gồm ancol metylic, ancol etylic và ancol isopropylic rồi hấp thụ toàn bộ sản phẩm cháy vào nước vôi trong dư được 80 gam kết tủa. Thể tích oxi (đktc) tối thiểu cần dùng là
A.16,8 lít. B.26,88 lít. C.23,52 lít. D.21,28 lít.
Đáp án đề thi thử THPT Quốc gia môn Hóa năm 2016- đề số 5

Tất cả nội dung bài viết. Các em hãy xem thêm và tải file chi tiết tại đây:Download

