Tham khảo đề thi thử THPT Quốc gia năm 2016 môn hóa đề số 3 có đáp án và lời giải chi tiết giúp các em thử sức với kỳ thi sắp tới.
Xem thêm: Đề thi thử THPT Quốc gia môn Hóa
Cho nguyên tử khối của các nguyên tố: H: 1; Li: 7; C: 12; N: 14; O: 16; Na: 23;Mg: 24;Al: 27; S: 32; Cl: 35,5; K: 39; Ca:40; Cr: 52; Mn: 55; Fe: 56; Cu: 64; Zn: 65;Br: 80; Ba: 137; Ag: 108;Cs: 133
Câu 1. Hấp thụ hoàn toàn 0,672 l CO
(dktc) vào 1 l dung dịch gồm NaOH 0,01M và Ca(OH)
0,02M thu được x gam kết tủa. Giá trị của x là :
A.0,75 B.1,25 C.2,00 D.1,00
Câu 2. Trộn KMnO
và KClO
với 1 lượng MnO
trong bình kín thu được hỗn hợp X. Lấy 52,550g X đem nung nóng sau thời gian thì được hỗn hợp rắn Y và V lít O
.Biết KClO
bị nhiệt phân hoàn toàn tạo 14,9g KCl chiếm 36,315% khối lượng Y. Sau đó cho toàn bộ Y tác dụng với HCl đặc dư nung nóng , sau phản ứng cô cạn thu được 51,275g muối khan. Hiệu suất của quá trình nhiệt phân muối KMnO
là :
A.62,5% B.75% C.91,5% D.80%
Câu 3.Cho các thí nghiệm sau:
(a) Đốt H
S trong O
dư. (b) Đun nóng dung dịch bão hòa NH
Cl và NaNO
.
(c) Đốt P trong O
dư. (d) Dẫn khí F
vào NaOH loãng.
(e) Cho NH
tiếp xúc với CrO
(g) Cho H
SO
loãng vào Na
S
O
.
Số thí nghiệm tạo ra chất khí là:
A.5 B.3 C.4 D.2
Câu 4. Điện phân dung dịch hỗn hợp chứa 0,1 mol FeCl
; 0,2 mol CuCl
; 0,1 mol HCl ( điện cực trơ , màng ngăn xốp). Khi ở catot bắt đầu sủi bọt thì ngừng điện phân. Tại thời điểm này khối lượng catot đã tăng lên:
A.12,8 B.18,4 C.0,0 D.5,6
Câu 5. Hỗn hợp X gồm 1 đipeptit, 1 tripeptit đều cấu tạo từ 1 loại a-amino axit no mạch hở có 1 nhóm –NH
và 1 nhóm –COOH trong phân tử. Trong X nguyên tố N chiếm 15,135% về khối lượng hỗn hợp. Cho 44,4g hỗn hợp X tác dụng với 600 ml dung dịch NaOH 1M (dư) đun nóng thu được dung dịch Y. Cô cạn Y thu lượng chất rắn khan là:
A.68,04 B.64,80 C.85,05 D.51,03
Câu 6.Cho phenol (C
H
OH) lần lượt tác dụng với (CH
CO)
O và các dung dịch : NaOH ; HCl ; Br
; HNO
; CH
COOH. Số trường hợp xảy ra phản ứng là:
A.4 B.2 C.1 D.3
Câu 7. Lần lượt thực hiện các phản ứng sục khí Clo vào dung dịch sau: Fe
(SO
)
; (NaCrO
+ NaOH) ; FeSO
; NaOH ; CuCl
; CrCl
. Số thí nghiệm làm thay đổi số oxi hóa của nguyên tố kim loại trong hợp chất là:
A.4 B.5 C.6 D.3
Câu 8. Phát biểu nào sau đây đúng:
A. Khả năng phản ứng của Cl
kém hơn O
.
B. 1 ứng dụng của ozon là điều chế oxi trong phòng thí nghiệm.
C. Nitrophotka là hỗn hợp cả NH
H
PO
và KNO
.
D.Trong phòng thí nghiệm các khí: N
;O
;Cl
có thể thu bằng cách đẩy nước.
Câu 9. Cho mẫu kim loại Ba vào 500 ml dung dịch Al
(SO
)
0,1M. Sau phản ứng thu được dung dịch X, kết tủa Y và khí Z. Khối lượng dung dịch X giảm đi so với ban đầu là 19,59g. Sục từ từ đến dư CO
vào X thấy xuất hiện m gam kết tủa. Giá tri của m gần nhất với:
A. 3,10 B.2,30 C.1,60 D.4,0
Câu 10. Có bao nhiêu amin bậc 1 có cùng công thức phân tử C
H
N:
A. 7 B.5 C.8 D.6
Câu 11. a mol chất béo X có thể cộng với tối đa 4 mol Br
. Đốt cháy hoàn toàn a mol X thu được b mol nước và V lít CO
(dktc). Mối liên hệ giữa V với a,b là:
A.V= 22,4(b-6a) B.V=22,4(b-7a) C. V=22,4(b+7a) D. V=22,4(b+6a)
Câu 12. Số đồng phân axit có CTPT là C
H
O
là:
A.3 B.1 C.2 D.4
Câu 13. Đốt cháy hỗn hợp gồm 2,4g Mg ; 4,48g Fe với hỗn hợp X gồm có Cl
và O
; sau phản ứng chỉ thu được hỗn hợp Y gồm các oxit và muối clorua( không có khí dư). Hòa tan Y vào lượng vừa đủ 120 ml HCl 2M thu được dung dịch Z. Cho AgNO
dư vào Z thu được 61,01g kết tủa. Phần trăm V của O
trong X là:
A.51,72% B.53,85% C.46,15% D.76,70%
Câu 14.Chất (CH
)
CH-CH(NH
)-COOH có tên là:
A. axit-2-metyl-3-aminobutanoic B. axit-3-metyl-2-aminobutanoic
C. axit-2-amino-3-metylbutanoic D. axit-3-amino-2-metylbutanoic
Câu 15. Cho các phản ứng sau : (1) Ca(OH)
dư + NaHCO
; (2) NaHCO
dư + Ca(OH)
; (3) Ca(HCO
)
dư + NaOH ; (4) Ca(OH)
+ Ca(HCO
)
. Những phản ứng có phương trình ion rút gọn là: Ca
+ HCO
+ OH
® CaCO
+ H
O
A.(2)(3)(4) B. (1)(2)(3) C.(1)(3)(4) D.(1)(2)(4)
Câu 16. Chất hữu cơ Y có CTPT là C
H
. Khi cho Y tác dụng với dung dịch Brom thu được 2 chất hữu cơ Y
và Y
, trong đó Y
là 1,3-diBrom-2,2-dimetylpropan.Hãy cho biết tên của Y
:
A.2,3-dibrom-2-metylbutan B. 1,3-dibrom-3-metylbutan
C. 1,3-dibrompentan D. 1,3-dibrom-2-metylbutan
Câu 17. Hỗn hợp rắn A gồm Ca(HCO
) ; CaCO
; NaHCO
; Na
CO
. Nung A đến khối lượng không đổi được chất rắn B gồm:
A. CaCO
và Na
O B. CaO và Na
O C. CaCO
và Na
CO
D.CaO và Na
CO
Câu 18.Cho 11,04g hỗn hợp X gồm FeO ; Fe
O
; S ; FeS
; CuS trong đó O chiếm 14,5% về khối lượng. Cho X tác dụng vừa đủ với H
SO
đặc nóng sinh ra 0,31 mol SO
và dung dịch Y. Nhúng thanh Mg dư vào Y sau khí các phản ứng xảy ra hoàn toàn lấy thanh Mg ra cân lại tăng 2,8g ( giả sử 100% kim loại tạo ra bám hết vào thanh Mg).Đốt hoàn toàn m g X bằng lượng vừa đủ V(lit) (dktc) hỗn hợp A gồm O
và O
có tỉ khối so với H
là 20. Giá trị của V là:
A. 2,7776 B.2,0608 C.2,9568 D.5,9136
Câu 19.Tinh bột , xenlulose ; saccarose đều có khả năng phản ứng với:
A. Hòa tan Cu(OH)
B. trùng ngưng C.tráng gương D. Thủy phân
Câu 20. Phát biểu nào sau đây sai:
A. Ở nhiệt độ thường, tất cả các kim loại kiềm thổ đều tác dụng với nước.
B. Dung dịch Na
CO
và NaHCO
đều thủy phân cho môi trường kiềm
C. Nhôm bền trong không khí và nước do có màng oxit Al
O
bảo vệ.
D. Theo chiều tăng của điện tích hạt nhân thì nhiệt độ nóng chảy của kim loại kiềm giảm dần.
Câu 21. Hợp chất hữu cơ X mạch hở có phân tử khối là 56. Biết khi đốt cháy X bằng oxi thu được sản phẩm chỉ có CO
và H
O , X làm mất màu dung dịch Brom. Số CTCT thỏa mãn là:
A.5 B.3 C.2 D.4
Câu 22. Hòa tan hết 1 lượng S và 0,01 mol Cu
S trong HNO
đặc nóng sau phản ứng thu được dung dịch chứa 1 chất tan duy nhất và sản phẩm khử là NO
duy nhất. Hấp thụ hết lượng NO
này bằng 200 ml dung dịch NaOH 1M, cô cạn dung dịch sau phản ứng thì được m gam chất rắn khan. Giá trị của m là:
A.15,2 B.12,64 C.13,92 D.18,4
Câu 23. Cho cân bằng hóa học : 2NO
(khí) ↔ N
O
(khí) . ∆H = -58 kJ. Trong đó : NO
là khí màu đỏ ; N
O
không màu. Phát biểu nào sau đâu không đúng:
A.Ngâm bình trong nước đá, màu nâu của bình đậm hơn.
B. Giảm áp suất chung của hệ, màu của hỗn hợp đậm hơn.
C. Thêm vài giọt dung dịch NaOH vào bình phản ứng, màu của hỗn hợp đậm hơn.
D. Phản ứng nghịch thu nhiệt.
Câu 24.Nguyên tử R tạo được Cation R
. Cấu hình e của R
ở trạng thái cơ bản là 3p
. Tổng số hạt mang điện trong R là:
A. 18 B.22 C.38 D.19
Câu 25. Cho các hidrocacbon: eten ; axetilen ; benzen ; toluen ; isopentan ; Stiren. Số chất làm mất màu dung dịch KMnO
là:
A.4 B.5 C.6 D.3
Câu 26. Cho các phản ứng sau : (1) (CH
)
NH + NH
Cl ; (2) C
H
CH
NH
+ C
H
NH
Cl ; (3) CH
NH
Cl + NH
; (4) C
H
NH
Cl + NH
. Các phản ứng xảy ra là:
A.(1)(2)(4) B. (2)(3)(4) C. (1)(2)(3) D. (1)(3)(4)
Câu 27.Hòa tan a(gam) Fe vào dung dịch HCl thu được 2,24 l khí (dktc) và dung dịch D. Cô cạn D thu được m (gam) muối khan. Cho lượng muối trên vào 160 ml ( KMnO
/ H
SO
) 0,25M sau phản ứng hoàn toàn thu được V (lit) khí. Giá trị của V là:
A. 0,336 B.0,28 C. 2,24 D.1,12
Câu 28. Công thức chung của hidrocacbon là C
H
. Mối liên hệ giữa x và y là:
A. y ≤ 2x + 2 B.y = 2x + 2 C. y=2x D. y ≥ 2x – 2
Câu 29. Hỗn hợp X gồm 2 este đơn chức. Cho 0,5 mol X tác dụng với dung dịch AgNO
/NH
dư thu được 43,2g Ag. Cho 14,08g X tác dụng với KOH vừa đủ thu được hỗn hợp 2 muối của 2 axit đồng đẳng liên tiếp và 8,256 gam hỗn hợp ancol no đơn chức đồng đẳng liên tiếp , mạch hở. Công thức của 2 ancol là:
A. C
H
OH và C
H
OH B. CH
OH và C
H
OH
C. C
H
OH và C
H
OH D. C
H
OH và C
H
OH
Câu 30.Cho m gam tinh bột lên men để sản xuất ancol etylic, toàn bộ lượng CO
sinh ra cho qua dung dịch Ca(OH)
dư thu được 750 gam kết tủa. Biết hiệu suất mỗi giai đoạn lên men là 80%. Giá trị của m là:
A. 1054,7 B. 949,2 C. 765,5 D. 759,4
Câu 31. Peptit X mạch hở có công thức C
H
O
N
. Thủy phân hoàn toàn 0,1 mol X trong dung dịch NaOH đun nóng thu được m gam hỗn hợp muối của các α-amino axit ( các amino axit đều chứa 1 nhóm COOH và 1 nhóm NH
. Giá trị của m là:
A. 51,2 B. 47,2 C. 49,4 D. 49,0
Câu 32. Cho các chất sau : H
O ; C
H
OH; CH
COOH ; HCOOH ; C
H
OH. Chiều tăng dần độ linh động của nguyên tử H trong các nhóm chức của 4 chất là:
A. H
O ; C
H
OH ; C
H
OH ; HCOOH ; CH
COOH.
B. C
H
OH ; H
O ; C
H
OH ; CH
COOH ;HCOOH.
C. C
H
OH ; H
O ; C
H
OH ; HCOOH ; CH
COOH.
D. H
O ; C
H
OH ; C
H
OH ; CH
COOH ;HCOOH.
Câu 33. Cho các chất sau : axetilen ; axit fomic ; fomandehit ; phenyl fomat ; glucose ; andehit acetic ; metyl axetat ; natri fomat ; aceton. Số chất có thể tham gia phản ứng tráng gương là:
A.9 B.6 C.7 D.8
Câu 34. Cho 13,35g Alanin vào dung dịch NaOH thu được dung dịch Y. Dung dịch Y tác dụng vừa đủ với 250 ml dung dịch HCl 1M thu được dung dịch Z. Cô cạn dung dịch Z thu được bao nhiêu gam muối khan:
A. 18,825 B.35,245 C.24,675 D.18,675
Câu 35. Dãy gồm các chất đều phản ứng với HCOOH là:
A.CH
NH
; C
H
OH ; KOH ; NaCl B. NH
; K ; Cu ; NaOH ; H
;O
C. Na
O ; NaCl ; Fe ; CH
OH ; C
H
Cl D. AgNO
/NH
;Mg;C
H
OH;KOH; Na
CO
Câu 36. Để bảo quản Na người ta ngâm Na trong:
A. nước B.Dầu hỏa C. rượu etylic D. phenol lỏng
Câu 37. Cho các chất sau : FeCO
;FeS ;Fe
O
;Fe(OH)
. Nếu hòa tan cùng số mol mỗi chất vào dung dịch H
SO
đặc nóng dư thì chất tạo ra số mol khí lớn nhất là:
A.FeCO
B.Fe(OH)
C.Fe
O
D.FeS
Câu 38. Trộn 300 gam dung dịch Ba(OH)
1,254% với 500 ml dung dịch chứa H
PO
0,04M và H
SO
0,02M. Khối lượng các muối thu được sau phản ứng là:
A.5,56 B.3,262 C.5,91 D.4,978
Câu 39. Crackinh hoàn toàn V lít ankan X thu được hỗn hợp Y gồm 0,1V lít C
H
; 0,6V lít CH
; 1,8V lít các hidrocacbon khác. Tỉ khối của Y so với H
là 14,4. Dẫn 1 mol Y đi qua bình chứa dung dịch Brom dư , phản ứng kết thúc thấy khối lượng bình tăng m gam. Biết các thể tích khí đo ở cùng điều kiện, chỉ có ankan tham gia phản ứng crackinh. Giá trị của m là:
A. 22,3 B.23,2 C.19,6 D.21,6
Câu 40. Hãy cho biết phản ứng nào sau đây không xảy ra:
A. CH
CH
OH ® anken ( H
SO
đặc,170
C) B. CH
OH + C
H
OH ® ete
C. CH
CH
OH ® ete ( H
SO
đặc,140
C) D. CH
OH ® ete ( H
SO
đặc,140
C)
Câu 41. Hơi thủy ngân rất độc , vì vậy khí vỡ nhiệt kế , chất bột được rắc lên thủy ngân và sau đó gom lại là:
A.Cát B.Lưu huỳnh C. muối ăn D.Vôi sống
Câu 42. Polime không có nguồn gốc từ xenlulose là:
A. Sợi bông B.tơ tằm C.tơ visco D. Tơ xenlulose triacetat
Câu 43. Trong số các dung dịch Cu(NO
)
; Fe(NO
)
; AgNO
; Pb(NO
)
; Zn(NO
)
; FeCl
. Số dung dịch phản ứng được với H
S là:
A.6 B.5 C.3 D.4
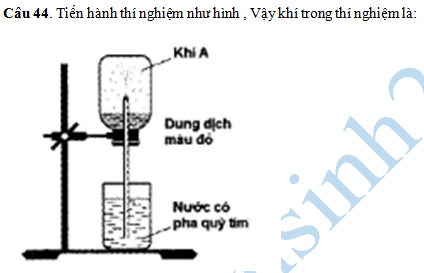
A.CO
B.HCl C.H
D.NH
Câu 45. Cho phương trình : X + NaOH ® Na
SO
+ H
O (1). Hãy cho biết có bao nhiêu chất X thỏa mãn phương trình (1)?
A.3 B.1 C.4 D.2
Câu 46. Đốt cháy 1 hỗn hợp no mạch hở X ( gồm 1 axit và 1 andehit có cùng số C) thu được số mol H
O bằng số mol X). Nếu cho X phản ứng với AgNO
/NH
thu được số mol Ag gấp 2 lần số mol X.Phần trăm khối lượng Oxi trong axit là:
A.55,17% B.69,56% C.53,33% D.71,11%
Câu 47. Trong các kim loại ( Na;Al;Ba;Fe;Cr), số kim loại hòa tan trong H
O dư ở nhiệt độ thường là:
A.2 B.3 C.1 D.4
Câu 48. X có vòng benzen và có CTPT C
H
O
. X tác dụng dễ dàng với dung dịch brom thu được chất Y C
H
O
Br
. Mặt khác , cho X tác dụng với NaHCO
thu được muối Z có công thức phân tử C
H
O
Na. X có bao nhiêu công thức cấu tạo:
A.4 B.3 C.5 D.1
Câu 49. Kim loại nào sau đây có nhiệt độ nóng chảy thấp nhất:
A.Kali B.Thủy ngân C.Rubidi D.Cesi
Câu 50. Trộn lẫn 100 ml dung dịch NaOH 0,01M và 200 ml HCl 0,02M thu được dung dịch Y. Dung dịch Y có pH là:
A. 1,8 B.3,0 C. 4,2 D. 2,0
Đáp án đề thi thử THPT Quốc gia môn Hóa năm 2016 – Đề số 3
|
Câu |
Đáp án |
Câu |
Đáp án |
Câu |
Đáp án |
Câu |
Đáp án |
Câu |
Đáp án |
|
1 |
C |
11 |
D |
21 |
A |
31 |
B |
41 |
B |
|
2 |
D |
12 |
C |
22 |
C |
32 |
B |
42 |
B |
|
3 |
A |
13 |
C |
23 |
A |
33 |
B |
43 |
D |
|
4 |
A |
14 |
C |
24 |
C |
34 |
C |
44 |
B |
|
5 |
B |
15 |
C |
25 |
A |
35 |
D |
45 |
A |
|
6 |
A |
16 |
B |
26 |
A |
36 |
B |
46 |
D |
|
7 |
D |
17 |
D |
27 |
D |
37 |
D |
47 |
A |
|
8 |
D |
18 |
B |
28 |
A |
38 |
C |
48 |
C |
|
9 |
C |
19 |
D |
29 |
A |
39 |
C |
49 |
B |
|
10 |
C |
20 |
A |
30 |
B |
40 |
B |
50 |
D |
Lời giài chi tiết các em xem trong file đính kèm.
Tất cả nội dung bài viết. Các em hãy xem thêm và tải file chi tiết tại đây:Download

