Đề thi thử THPT Quốc gia môn Hóa năm 2016 đề số 10 sẽ giúp các em có thêm nhiều dạng bài tập để chuẩn bị tốt cho kì thi quan trọng này.Đề thi gồm 50 câu hỏi và đáp án hướng dẫn các em xem bên dưới
Xem thêm: Đề thi thử THPT Quốc gia môn Hóa
Cho biết khối lượng nguyên tử (theo u) của các nguyên tố:
H = 1; Li = 7; C = 12; N = 14; O = 16; Na = 23; Mg = 24; Al = 27; P = 31; S = 32; Cl = 35,5; K = 39;
Ca = 40; Cr=52, Fe = 56; Cu = 64; Zn = 65; As = 75; Br = 80; Rb = 85,5; Ag = 108; Ba = 137, I=127.
Câu 1: Tính khối lượng fructozơ cần dùng để hòa tan vừa hết 25,872 gam Cu(OH)
. Giả sử hiệu suất phản ứng là 100%.
A. 32,34 gam. B. 316,8 gam.
C. 95,04 gam. D. 60,92 gam.
Câu 2: Trường hợp nào sau đây không xảy ra phương trình phản ứng?
A. Cho dung dịch FeCl
vào dung dịch AgF.
B. Cho dung dịch Fe(NO
)
vào dung dịch AgNO
.
C. Cho dung dịch Fe(NO
)
vào dung dịch HF.
D. Cho dung dịch Fe(NO
)
vào dung dịch AgNO
.
Câu 3: Lượng triolein cần để điều chế 5,88 kg glixerol với hiệu suất phản ứng 85% là
A. 66,47 kg. B. 56,5 kg.
C. 48,025 kg. D. 22,26 kg.
Câu 4: Dùng ba ống nghiệm đánh số 1, 2, 3 cho hóa chất vào các ống nghiệm theo bảng sau:
Bằng đồng hồ bấm giây, người ta đo khoảng thời gian từ lúc bắt đầu trộn dung dịch đến khi xuất hiện kết tủa, đối với kết quả ở ba ống nghiệm 1, 2, 3 người ta thu được ba giá trị t
, t
, t
. Khẳng định nào sau đây đúng?
|
Ống nghiệm |
Na S O |
H O |
H SO |
Thể tích chung |
Thời gian kết tủa |
|
1 |
4 giọt |
8 giọt |
1 giọt |
13 giọt |
t |
|
2 |
12 giọt |
0 giọt |
1 giọt |
13 giọt |
t |
|
3 |
8 giọt |
4 giọt |
1 giọt |
13 giọt |
t |
A. t
> t
> t
. B. t
< t
< t
.
C. t
> t
> t
. D. t
< t
< t
.
Câu 5: Hoà tan m gam Al(NO
)
vào nước được dung dịch X. Nếu cho 0,51mol KOH vào dung dịch X thu được 3x gam kết tủa. Mặt khác, nếu cho 0,57mol KOH vào dung dịch X thu được x gam kết tủa. Giá trị của m là
A. 21,30. B. 39,405.
C. 31,95. D. 42,60.
Câu 6: Để chứng minh Cl
vừa có tính khử vừa có tính oxi hóa, người ta cho Cl
tác dụng với
A. dung dịch FeCl
. B. dây sắt nóng đỏ.
C. dung dịch NaOH loãng. D. dung dịch KI.
Câu 7: Nung nóng từng cặp chất sau trong bình kín ở nhiệt độ cao:
(1) Fe và S (rắn); (2) Au và O
(khí); (3) Cu và Cr
O
;
(4) Ag + Cl
(khí); (5) Mg và CO
(khí); (6) Al và C (cacbon).
Số trường hợp xảy ra phản ứng oxi hóa kim loại là
A. 5. B. 3.
C. 2. D. 4.
Câu 8: Xét phản ứng este hoá giữa CH
COOH và C
H
OH. Nếu phản ứng được khởi đầu với 1 mol axit và 1 mol C
H
OH, ta có đường biểu diễn số mol este thu được theo thời gian:
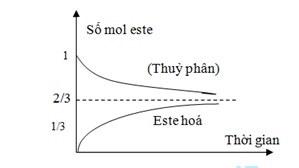
Hiệu suất của phản ứng este hóa đạt giá trị cực đại là
A. 88,8%. B. 33,3%.
C. 66,7%. D. 55,0%.
Câu 9: Trong phòng thí nghiệm, để nhận biết được trong một dung dịch có tồn tại ion Br
hay không, người ta hay cho vào ống nghiệm chứa dung dịch đó một ít bột MnO
và vài giọt H
SO
đặc sau đó đun nóng. Hiện tượng xảy ra là
A. có hơi màu tím bay ra. B. có hơi màu nâu đỏ bay ra.
C. có kết tủa màu vàng. D. có kết tủa màu xanh.
Câu 10: Tỉ khối hơi của hỗn hợp 2 anđehit X, Y đối với heli bằng 14,5 với mọi tỉ lệ mol giữa X và Y. Cho 17,4g hỗn hợp X và Y (tỉ lệ mol 1:1) vào dung dịch AgNO
/NH
dư thu được số mol Ag tối đa là
A. 0,6. B. 0,8.
C. 1,2. D. 0,9.
Câu 11: Trong công nghiệp, quá trình sản xuất nào sau đây là sai?
A. Điện phân dung dịch muối ăn (nồng độ từ 15% – 20%) trong thùng điện phân có màng ngăn để sản xuất nước Gia-ven.
B. Điện phân MgCl
nóng chảy để sản xuất magie.
C. Điện phân hỗn hợp KF và HF (hỗn hợp ở thể lỏng) để sản xuất khí flo.
D. Điện phân hỗn hợp Al
O
và 3NaF.AlF
nóng chảy để sản xuất nhôm.
Câu 12: Cho 7 gam axit cacboxylic đơn chức X vào dung dịch chứa 7 gam KOH thì thu được dung dịch có chứa 11,75 gam chất tan. Axit cacboxylic X là
A. C
H
COOH. B. HCOOH.
C. CH
COOH. D. C
H
COH.
Câu 13: Khi thêm từ từ nước vào một cốc đựng dung dịch CH
COOH thì
(1): số phân tử CH
COOH không thay đổi.
(2): độ điện li của CH
COOH sẽ tăng lên.
(3): độ dẫn điện của dung dịch sẽ tăng lên.
(4): pH của dung dịch sẽ không thay đổi.
(5): cân bằng sẽ dịch chuyển theo chiều làm tạo thêm ion CH
COO
.
Chọn ý đúng trong 5 ý trên.
A. (2), (4), (5). B. (1), (2), (4).
C. (2), (5). D. (2), (3), (5).
Câu 14: Để khử hoàn toàn hỗn hợp gồm 78,88g Fe
O
và 43,86g Al
O
cần vừa đủ V lit CO (đktc). Giá trị của V là
A. 30,464. B. 59,360.
C. 10,155. D. 61,376.
Câu 15: Trong dung dịch, cation X
oxi hóa được kim loại Y. Khi nhúng hai thanh kim loại X và Y được nối với nhau bằng dây dẫn điện vào một dung dịch chất điện li H
SO
loãng thì
A. ở anot xảy ra quá trình khử: 2H
+2e ®H
.
B. có dòng electron di chuyển từ kim loại Y đến kim loại X.
C. kim loại X bị ăn mòn điện hoá, Y không bị ăn mòn điện hoá.
D. ở catot xảy ra quá trình oxi hóa: 2X ® X
+2e
Câu 16: Paracetamol là một hoạt chất có trong thuốc giảm đau. Paracetamol được tạo thành khi trùng ngưng axit axetic với p-aminophenol với tỉ lệ mol 1:1. Chọn phát biểu đúng về paracetamol.
A. Trong phân tử paracetamol có chứa liên kết peptit.
B. Paracetamol có thể làm mất màu dung dịch brom.
C. Paracetamol có thể tác dụng với Cu(OH)
tạo thành hợp chất màu tím.
D. Dung dịch paracetamol (trong nước) làm xanh giấy quì.
Câu 17: Cho hỗn hợp kim loại gồm x mol Na và y mol Ba vào nước dư được V lít H
(đktc) và dung dịch X. Khi cho CO
hấp thụ từ từ đến dư vào dung dịch X, kết quả thí nghiệm được biểu diễn trên đồ thị sau:
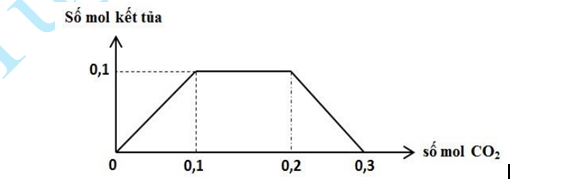
Tỉ lệ x : y là:
A. 2:1. B. 1:3.
C. 1:1. D. 1:2.
Câu 18: Cho một thanh Zn vào 200ml dung dịch CrCl
1M. Sau khi các phản ứng xảy ra hoàn toàn, lấy thanh Zn ra đem cân thì khối lượng thanh kẽm sẽ
A. giảm 9,1 gam. B. giảm 13 gam.
C. giảm 6,5 gam. D. giảm 18,2 gam.
Câu 19: Cho các phát biểu sau:
1) Tinh thể SiO
chỉ chứa liên kết đơn.
2) Trong nhóm IA, liti có nhiệt độ sôi cao nhất.
3) Phân supephotphat kép có chứa Ca(HPO
)
và CaSO
.
4) Trong nhóm halogen, flo có nhiệt độ sôi thấp nhất.
5) Bón nhiều phân đạm amoni sẽ làm cho đất chua.
6) Kim cương và than chì là hai dạng thù hình của cacbon.
7) Ở 100
C, phân tử lưu huỳnh có 8 nguyên tử liên kết cộng hóa trị với nhau tạo thành mạch vòng.
Số phát biểu đúng là:
A. 6. B. 7.
C. 4. D. 5.
Câu 20: Cho m gam bột Cu vào 200 ml dung dịch AgNO
0,2M, sau một thời gian thu được 3,12 gam chất rắn X và dung dịch Y. Cho 1,95 gam Zn vào dung dịch Y đến phản ứng hoàn toàn thu được 3,45gam chất rắn Z và dung dịch chứa 1 muối duy nhất. Giá trị của m là
A. 0,64. B. 1,28.
C. 1,92. D. 1,6.
Câu 21: Phát biểu nào sau đây là đúng?
A. Amilozơ có cấu trúc mạch không phân nhánh.
B. Glucozơ bị oxi hoá bởi H
(xúc tác Ni, t
).
C. Thuỷ phân saccarozơ chỉ cho glucozơ.
D. Trong mỗi mắt xích xenlulozơ có 2 nhóm -OH.
Câu 22: Cho m gam bột Fe vào 50 ml dung dịch Cu(NO
)
1M, sau phản ứng thu được dung dịch X và 4,88 gam chất rắn Y. Cho 4,55 gam bột Zn vào dung dịch X, kết thúc phản ứng thu được 4,1 gam chất rắn Z và dung dịch chứa một muối duy nhất. Giá trị của m là
A. 4,48. B. 2,80.
C. 5,60. D. 8,40.
Câu 23: Thu 3 khí O
, HCl và SO
vào đầy 3 lọ có dung tích và chiều cao như nhau rồi úp ngược 3 miệng lọ vào 3 chậu nước thấy nước dâng lên trong các lọ theo thứ tự là h
, h
, h
. Độ cao nước dâng lên giảm theo thứ tự là
A. h
> h
> h
. B. h
> h
> h
.
C. h
> h
> h
. D. h
> h
> h
.
Câu 24: Hỗn hợp khí X gồm amin no, đơn chức, mạch hở Y và ankin Z. Đốt cháy hoàn toàn 0,2 mol X, thu được 0,45 mol CO
và 0,375 mol H
O. Công thức phân tử của Y và Z là
A. C
H
N và C
H
. B. C
H
N và C
H
.
C. C
H
N và C
H
. D. C
H
N và C
H
.
Câu 25: Số liên kết cộng hóa trị có trong một phân tử phenylamoni clorua là
A. 16. B. 17.
C. 18. D. 19.
Câu 26: Cho 2,5 kg glucozơ chứa 20% tạp chất lên men thành ancol etylic. Tính thể tích ancol 40
thu được Biết khối lượng riêng của ancol etylic là 0,8g/ml và quá trình chế biến hao hụt 10%.
A. 3194,4 ml. B. 27850 ml.
C. 2875,0 ml. D. 23000 ml.
Câu 27: Natri silicat có thể được tạo thành bằng cách nào dưới đây?
A. Đun SiO
với NaOH nóng chảy.
B.Cho SiO
tác dụng với dung dịch NaOH loãng.
C. Cho Si tác dụng với dung dịch NaCl.
D. Cho dung dịch K
SiO
tác dụng với dung dịch NaHCO
.
Câu 28: Để trung hoà m gam hỗn hợp X gồm CH
COOH, CH
(COOH)
, CH(COOH)
, C(COOH)
cần 540ml dung dịch NaOH 2M. Đốt cháy hoàn toàn m gam hỗn hợp X cần 17,92 lít O
(đktc). Giá trị của m là
A. 54,68. B. 52,16.
C. 53,92. D. 51,88.
Câu 29: Kim loại nào sau đây có thể tan được trong dung dịch NaOH đặc?
A. Ag. B. Fe.
C. Al. D. Mg.
Câu 30: Nhiệt nhôm hoàn toàn m gam hỗn hợp X gồm Al, Fe
O
(không có không khí) thu được hỗn hợp Y. Chia Y thành hai phần:
Phần 1: Cho tác dụng với NaOH dư thu được 1,008 lít H
(đktc) và còn lại 5,04 gam chất rắn không tan.
Phần 2: có khối lượng 29,79 gam, cho tác dụng với dung dịch HNO
loãng dư thu được 8,064 lít NO (đktc, sản phẩm khử duy nhất).
Giá trị của m và công thức của oxit sắt là
A. 39,72 gam và FeO. B. 39,72 gam và Fe
O
.
C. 38,91 gam và FeO. D. 36,48 gam và Fe
O
.
Câu 31: Kiểu liên kết giữa các gốc glucozơ trong amilozơ là:
A. α-1,6-glicozit. B. α -1,2-glicozit.
C.β-1,4-glicozit. D.α -1,4-glicozit.
Câu 32: Một bình kín chứa hỗn hợp X gồm 0,06 mol axetilen; 0,09 mol vinylaxetilen; 0,16 mol H
và một ít bột Ni. Nung hỗn hợp X thu được hỗn hợp Y gồm 7 hiđrocacbon (không chứa but-1-in) có tỉ khối hơi đối với H
là 328/15. Cho toàn bộ hỗn hợp Y đi qua bình đựng dung dịch AgNO
/NH
dư, thu được m gam kết tủa vàng nhạt và 1,792 lít hỗn hợp khí Z thoát ra khỏi bình. Để làm no hoàn toàn hỗn hợp Z cần vừa đúng 50 ml dung dịch Br
1M. Các phản ứng xảy ra hoàn toàn. Giá trị của m là
A. 28,71. B. 14,37.
C. 13,56. D. 15,18.
Câu 33: Thực hiện các thí nghiệm sau :
(1) Sục khí SO
vào dung dịch K
Cr
O
trong H
SO
loãng. (2) Sục khí SO
vào dung dịch H
S.
(3) Sục khí SO
vào dung dịch Ca(OH)
. (4) Cho KMnO
vào dung dịch HCl đặc.
(5) Cho SiO
vào dung dịch HF. (6) Cho CrO
vào dung dịch NaOH.
Số thí nghiệm có phản ứng oxi hóa – khử xảy ra là
A. 4. B. 6.
C. 5. D. 3.
Câu 34: Cho 52,8 gam hỗn hợp rắn X gồm Fe
O
, Cu(NO
)
và Cu vào dung dịch chứa 0,6 mol H
SO
, đun nóng. Sau khi kết phản ứng phản ứng thu được khí NO (sản phẩm khử duy nhất) và dung dịch Y chỉ chứa 2 muối có khối lượng m gam. Cho bột Cu vào dung dịch Y không thấy phản ứng hóa học xảy ra. Giá trị của m là
A. 42,8. B. 46,6.
C. 52,8. D. 54,6.
Câu 35: Cho m gam anilin tác dụng hết với dung dịch Br
thu được 9,9 gam kết tủa. Giá trị của m là
A. 0,93. B. 2,79.
C. 1,86. D. 3,72.
Câu 36: Cho kim loại crom tác dụng với lượng dư HNO
đặc, sau phản ứng thấy thoát ra 6,72 lit khí NO (đktc). Khối lượng crom đã tham gia phản ứng là
A. 15,6 gam. B. 20 gam.
C. 14,8 gam. D. 12,5 gam.
Câu 37: Trước đây, Freon được dùng làm chất sinh hàn trong tủ lạnh và máy điều hòa nhiệt độ. Từ năm 1996, Freon đã bị cấm sử dụng, nguyên nhân chính là do khi thải vào khí quyển:
A. freon phá hủy tầng ozon. B. freon gây ra hiệu ứng nhà kính.
C. freon gây ra mưa axit. D. freon gây ra hiện tượng El Nino.
Câu 38: Hỗn hợp X gồm etilen glicol, ancol etylic, ancol propylic và hexan trong đó số mol hexan bằng số mol etilen glicol. Cho m gam hỗn hợp X tác dụng với Na dư thu được 0,4032 lít H
(đktc). Mặt khác, đốt cháy hoàn toàn m gam hỗn hợp X cần 4,1664 lít O
(đktc). Giá trị của m là
A. 2,682. B. 1,788.
C. 2,235. D. 2,384.
Câu 39: Một dung dịch có chứa các ion: Mg
, Na
, Fe
Fe
, Cu
, Ba
, NO
,Cl
. Để nhận ra sự có mặt của ion Fe
trong dung dịch, người ta có thể dùng chất nào sau đây?
A. NaOH. B. NH
.
C. Na
CO
. D. HCl.
Câu 40: Tổng số khối của 2 nguyên tử X, Y là 34. Trong 2 nguyên tử X, Y, tổng số hạt mang điện nhiều hơn số hạt không mang điện là 14. Biết nguyên tử X là đồng vị của nguyên tử Y. Số khối của X và Y là
A. 13 và 21. B. 14 và 20.
C. 15 và 19. D. 16 và 18.
Câu 41: Thiếc (Sn) là một kim loại thuộc chu kì 4, nhóm IVA trong bảng tuần hoàn. Tổng số electron p trong một nguyên tử Sn là
A. 16. B. 22.
C. 20. D. 14.
Câu 42: Điện phân 250gam dung dịch CuSO
8% cho đến khi nồng độ dung dịch CuSO
giảm đi một nữa thì dừng lại. Khối lượng kim loại bám trên catốt là
A. 2,02 gam. B. 4,08 gam.
C. 6,12 gam. D. 5,07gam.
Câu 43: Chọn câu sai.
A. Sản phẩm của phản ứng trùng ngưng phenol với fomandehit trong môi trường axit là polime mạch không nhánh.
B. Sản phẩm của phản ứng trùng ngưng axit e – aminocaproic là polipeptit.
C. Sản phẩm của phản ứng trùng ngưng etylenglicol với axit terephtalic là polieste.
D. Sản phẩm của phản ứng trùng hợp caprolactam là poliamit.
Câu 44: Cho giản đồ năng lượng của phản ứng: 2 H
+O
2H
O
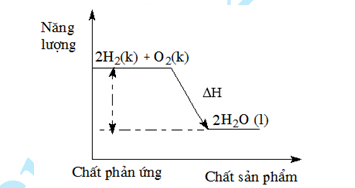
Kết luận nào sau đây về giá trị của các nhiệt phản ứng trên là đúng?
A. DH < 0 : phản ứng tỏa nhiệt. B. DH < 0 : phản ứng thu nhiệt.
C. DH > 0 : phản ứng tỏa nhiệt. D. DH > 0 : phản ứng thu nhiệt.
Câu 45: Cho 4 mol axit axetic tác dụng với hỗn hợp chứa 0,5 mol glixerol và 1 mol etilenglicol (xúc tác H
SO
). Tính khối lượng sản phẩm hữu cơ thu được. Biết rằng có 50% axit và 80% mỗi ancol phản ứng.
A. 312 gam. B. 156,7 gam.
C. 170,4 gam. D. 176,5 gam.
Câu 46: Số tetrapeptit tạo từ 3 α-aminoaxit: Alanin; Glyxin và Valin là
A. 30. B. 32.
C. 36. D. 34.
Câu 47: Hỗn hợp X gồm Na
O, Na
O
, Na
CO
, K
O, K
O
, K
CO
. Cho m gam hỗn hợp X tác dụng với dung dịch HCl dư thu được dung dịch Y chứa 50,85 gam chất tan gồm các chất tan có cùng nồng độ mol; 3,024 lít hỗn hợp khí Z (đktc) có tỉ khối so với hiđro là 20,889. Giá trị của m là
A. 30,492. B. 22,689.
C. 21,780. D. 29,040.
Câu 48: Trong số các chất: CH
COONa, Na
HPO
, NaHS, Al
(SO
)
, NaHSO
, CH
COONH
, Al(OH)
, Zn(OH)
, CrO
, HOOC-COONa, HOOC-CH
NH
Cl, AlF
. Số chất lưỡng tính là
A. 7. B. 9.
C. 8. D. 10.
Câu 49: Hỗn hợp A gồm peptit X và peptit Y (tỉ lệ số mol 1:3). X và Y cấu tạo từ 1 loại aminoaxit, tổng số nhóm -CO-NH- trong 2 phân tử X và Y là 5. Khi thủy phân hoàn toàn m gam A thu được 81 gam glyxin và 42,72g alanin. Giá trị của m là
A. 104,28. B. 109,5.
C. 116,28. D. 110,28.
Câu 50: Hợp chất nào sau đây không chứa lưu huỳnh?
A. Cao su Buna-S. B. Oleum.
C. Quặng pirit sắt. D. Cao su lưu hóa.
Đáp án đề thi thử THPT Quốc gia môn Hóa năm 2016- đề số 10

Tất cả nội dung bài viết. Các em hãy xem thêm và tải file chi tiết tại đây:Download

